
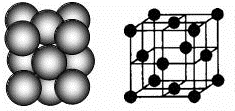
 银晶体的晶胞如图所示为面心立方最密堆积.设银原子的直径为d,用NA表示阿伏加德罗常数,在立方体的各个面的对角线上3个银原子彼此两两相切,M表示银的摩尔质量.则银晶体的密度
银晶体的晶胞如图所示为面心立方最密堆积.设银原子的直径为d,用NA表示阿伏加德罗常数,在立方体的各个面的对角线上3个银原子彼此两两相切,M表示银的摩尔质量.则银晶体的密度
| ||
| d3NA |
| ||
| d3NA |
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
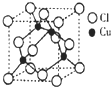 (2013?济南二模)金属铜的导电性仅次于银,大量用于电气工业.
(2013?济南二模)金属铜的导电性仅次于银,大量用于电气工业.查看答案和解析>>
科目:高中化学 来源: 题型:
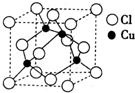 (2012?淄博一模)金属铜的导电性仅次于银,大量用于电气工业.
(2012?淄博一模)金属铜的导电性仅次于银,大量用于电气工业.查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省绵阳市涪城区南山中学高二(上)期中化学试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com