
【题目】取软锰矿石(主要成分为MnO2)116 g跟足量浓盐酸发生如下反应(杂质不参与反应)MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,制得22.4 L Cl2(标准状况),下列有关说法中不正确的是
MnCl2+Cl2↑+2H2O,制得22.4 L Cl2(标准状况),下列有关说法中不正确的是
A.这种软锰矿石中MnO2的质量分数为75%
B.被氧化的HCl的物质的量为4 mol
C.参加反应的HCl的质量为146 g
D.被还原的MnO2的物质的量为1 mol
【答案】B
【解析】
先计算氯气的物质的量,然后根据方程式中物质反应转化关系计算物质的作用及反应的物质的量或质量。
A.n(Cl2)=![]() =1mol,由MnO2+4HCl(浓)
=1mol,由MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O反应方程式可知:反应产生1molCl2,有1molMnO2参加反应,其质量为87g,则软锰矿石中MnO2的质量分数为
MnCl2+Cl2↑+2H2O反应方程式可知:反应产生1molCl2,有1molMnO2参加反应,其质量为87g,则软锰矿石中MnO2的质量分数为![]() ×100%=75%,A正确;
×100%=75%,A正确;
B.由反应可知,生成1molCl2气体时,2molHCl被氧化,B错误;
C.参加反应的HCl为4mol,其质量m(HCl)=4mol×36.5g/mol=146g,C正确;
D.在该反应中,Mn元素的化合价降低,被还原的MnO2的物质的量为1mol,D正确;
故合理选项是B。


科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:A(g)+3B(g)![]() 2C(g),有关下列图像说法的不正确的是( )
2C(g),有关下列图像说法的不正确的是( )
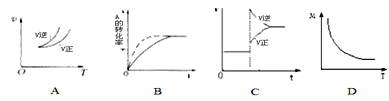
A. 依据图A可判断正反应为放热反应
B. 在图B中,虚线可表示使用了催化剂
C. 若正反应的△H<0,图C可表示升高温度使平衡向逆反应方向移动
D. 由图D中混合气体的平均相对分子质量随温度的变化情况,可推知正反应的△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予了对锂离子电池方面的研究作出贡献的约翰·B·古迪纳夫(John B.Goodenough)等三位科学家。已知可充电镍酸锂离子电池的工作原理如图所示,其总反应为:![]() 。下列说法不正确的是( )
。下列说法不正确的是( )
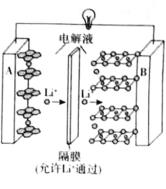
A.放电时,A电极为![]() 作原电池负极
作原电池负极
B.放电时,B电极反应式为![]()
C.充电时,A电极反应式为![]()
D.充电时,当电路中通过![]() 电子的电量时,A、B两极质量变化差为
电子的电量时,A、B两极质量变化差为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氧有机化合物是重要的化学工业原料。完成下列填空:
(1)工业上,乙醇可以通过粮食发酵制取,也可由乙烯在一定条件下和__________反应制取。
(2)乙醇催化氧化生成乙醛,将铜丝在空气中灼烧变黑后,迅速伸入乙醇中,观察到铜丝表面________________;反复上述多次操作后,闻到刺激性气味,说明有_____________生成。
(3)乙醛中的官能团为____________。乙醛与环氧乙烷(![]() )互为____________。
)互为____________。
(4)写出检验乙醛的化学反应方程式:_______________________________________,上述反应显示乙醛具有__________性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物,在标准状况下,其蒸气密度为2.054g/L,则其摩尔质量为_____________,又知4.6克该有机物完全燃烧生成二氧化碳2.24L(标准状况)和1.8克水,则该有机物的分子式为________,该有机物能与乙醇发生酯化反应,则该有机物的结构简式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2和CH4催化重整可制备合成气,对减缓燃料危机具有重要的意义,其反应历程示意图如图:

下列说法中错误的是( )
A.过程①→②是吸热反应
B.Ni是该反应的催化剂
C.过程①→②既有碳氧键的断裂,又有碳氧键的形成
D.反应的总化学方程式可表示为:CH4+CO2![]() 2CO+2H2
2CO+2H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物![]() 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:铜铝混合物![]() 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是
A. 溶液A和B均可以是盐酸或氢氧化钠溶液
B. 溶液A和B均可以选用稀硝酸
C. 若溶液B选用氯化铁溶液,则实验难以实现
D. 实验方案Ⅱ更便于实施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象与结论对应关系正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向盛有稀 | 试管口出现红棕色气体 | 溶液中的 |
B | 向某钠盐X溶液中加入盐酸,将产生的气体通入 | 有白色沉淀产生 | 反应生成的气体可能为 |
C | 向滴加酚酞的氨水中加蒸馏水稀释 | 溶液红色变浅 | 溶液中所有离子的浓度均减小 |
D | 用铂丝蘸取某溶液在酒精灯火焰上灼烧 | 直接观察,火焰呈黄色 | 溶液中的金属阳离子只有 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水三氯化铁呈棕红色,易潮解,100℃左右时升华,冷却后易凝华。下图是两名学生设计的用氯气与铁反应制备无水三氯化铁的实验装置。左边的反应装置相同,而右边的产品收集装置则不同,分别如(I)和(II)所示。试回答:
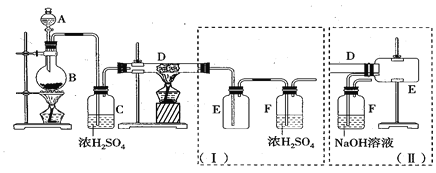
(1)A仪器的名称是_____________________;
(2)B中反应![]() 离子方程式为______________________;其中浓盐酸表现出的性质为________;若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制取Cl2,制得的Cl2体积总是小于1.12 L(标准状况)的原因是______________;
离子方程式为______________________;其中浓盐酸表现出的性质为________;若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制取Cl2,制得的Cl2体积总是小于1.12 L(标准状况)的原因是______________;
(3)气体通过装置C![]() 目的是________________;
目的是________________;
(4)D中的反应开始前,需进行的操作是___________,应采取的方法是__________________;
(5)写出最佳方法鉴别D中产物的离子方程式:__________________________________________;
(6)装置(I)的主要缺点是_______________________________________________;
(7)如果选用(II)装置来完成实验,则必须采取的改进措施是__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com