
【题目】用中和滴定法测定某盐酸的物质的量浓度。
(1)标准溶液应盛于___________(填“A”或“B”)滴定管中。
(2)若选用酚酞作指示剂,以0.1250 mol·L-1的标准氢氧化钠溶液滴定,如何判断滴定终点____________。
(3)实验数据记录如下表,请分析数据并计算,盐酸的物质的量浓度=_________mol·L-1。

滴定次数 | 待测溶液体积/mL | ||
标准碱液 | |||
滴定前读数/mL | 滴定后读数/mL | ||
1 | 20.00 | 0.00 | 16.02 |
2 | 20.00 | 0.00 | 15.98 |
3 | 20.00 | 0.00 | 16.00 |
科目:高中化学 来源: 题型:
【题目】被称为万能还原剂的 NaBH4 溶于水并和水反应: NaBH4+2H2O=NaBO2+4H2↑。下列说法中正确的是(NaBH4 中 H 为-1 价)
A. NaBH4 既是氧化剂又是还原剂 B. NaBH4 是氧化剂,H2O 是还原剂
C. 硼元素被氧化,氢元素被还原 D. 被氧化的元素与被还原的元素质量之比为 1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=2的X,Y,Z三种酸的溶液各1mL,分别加水稀释到1 000mL,其pH与溶液体积(V)的变化关系如图所示,下列说法错误的是( ) 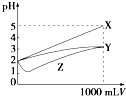
A.X是强酸,Y和Z是弱酸
B.稀释前的浓度大小为c(Z)>c(Y)>c(X)
C.稀释前电离程度大小为X>Y>Z
D.pH=2时,X,Y,Z都是稀溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸雨是含硫氧化物或含氮氧化物随雨写降到地面形成的,主要由化石燃料的大量使用造成,酸雨的治理响应了十九大报告提出的保护环境的基本国策。
(1)煤燃烧烟尘中的锰、铁等可使SO2转化为SO3发生反应2SO2(g)+O2(g)=2SO3(g)。某温度下将2.0molSO2和1.0molO2充入2L密闭容器中,若反应达平衡后,SO2的平衡转化率为0.6,则该反应的平衡常数为______。若升高温度,平衡常数减小,则该反应的ΔH_______0(填“>”、“=”“<”)。
(2)高浓度SO2和NO2在浓雾天气下反应生成了两种物质,其中一种为亚硝酸(HNO2),该过程发生反应的化学方程式为_________。
(3)洗涤含SO2的烟气,可以减少SO2排放,以下物质的溶液可作洗涤剂的是______。
a.氨气 b.苏打 c.氨水 d.明矾
(4)汽车尾气中含有NOx和CO,已知气缸中生成NO的反应为:N2(g)+O2(g) ![]() 2NO(g),则在恒容密闭容器中,下列说法中能说明该反应达到平衡状态的是________。
2NO(g),则在恒容密闭容器中,下列说法中能说明该反应达到平衡状态的是________。
a.混合气体的压强保持不变
b.混合气体的平均相对分子质量保持不变
c.NO质量分数保持不变
d.氧气的浓度保持不变
e.N2和NO正反应速率之比为1:2
(5)SO2可以变废为宝,利学家研究出了用电化学原理生产硫酸的新工艺(如下图所示),其阳极的电极反应式为__________。
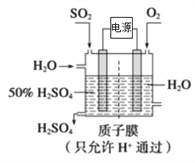
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,对于在恒容密闭容器中进行的反应:2SO2(g) +O2(g)2SO3(g), 下列叙述能充分说明该反应已经达到化学平衡状态的是( )
A.正、逆反应速率都等于零B.SO2、O2、SO3的浓度相等
C.SO2、O2、SO3在容器中共存D.SO2、O2、SO3的浓度均不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把400 mL NH4HCO3和Na2CO3的混合溶液分成两等份,取一份加入含a mol NaOH的溶液恰好反应完全;取另一份加入含b mol HCl的溶液恰好反应完全。该混合溶液中c(Na+)为( )
A. (10b-5a) mol·L-1 B. (b-0.5a) mol·L-1
C. (![]() -
-![]() ) mol·L-1 D. (5b-
) mol·L-1 D. (5b-![]() ) mol·L-1
) mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】前36号元素中的A、B、C、D、E、F的原子序数依次增大,只有前四种为短周期元素。A、B的原子核外s电子总数与p电子总数相等: C原子核外所有p轨道全满或半满: D元素的族序数与周期数的差为4;E是前四周期中电负性最小的元素:F在周期表的第七列。请根据以上相关信息,回答下列问题.
(1)A离子的电子共占据_____个轨道,A元素在自然界中的存在形态_____(a 只有化合态、b只有游离态、c都可能)。
(2)某人画的B的电子排布图如图![]() ,违背了________原理。
,违背了________原理。
(3)F位于______族,其基态原子的电子有_____种运动状态。
(4)CD3中心原子的杂化方式为____,用价层电子对互斥理论推测其分子空间构型为____,检验E元素的方法是___________。
(5)若某金属单质晶体中原子的堆积方式如图甲所示,其品胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.则晶胞中该原子的配位数为______,该单质晶体中原子的堆积方式为四种基本堆积方式中的________,若已知该金属的原子半径为dcm,NA代表阿伏加德罗常数,金属的相对原子质量为M,则该晶体的密度为________g/cm3(用字母表示)。
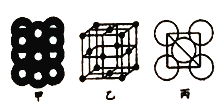
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com