
【题目】pH=2的X,Y,Z三种酸的溶液各1mL,分别加水稀释到1 000mL,其pH与溶液体积(V)的变化关系如图所示,下列说法错误的是( ) 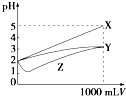
A.X是强酸,Y和Z是弱酸
B.稀释前的浓度大小为c(Z)>c(Y)>c(X)
C.稀释前电离程度大小为X>Y>Z
D.pH=2时,X,Y,Z都是稀溶液
【答案】D
【解析】解:A.加水稀释促进弱电解质电离,pH=2的三种酸,稀释1000倍后,如果该酸是强酸,则稀释后溶液pH=5,如果是弱酸,稀释后溶液的pH<5,根据图象知,稀释1000倍,X溶液的pH=5、Y和Z溶液pH小于5,所以X是强酸、Y和Z属于弱酸,故A正确;
B.pH相等时,弱酸浓度大于强酸,所以Y和Z浓度大于X,根据图象知,刚开始稀释时,Z的pH减小、Y的pH增大,说明Z是浓溶液、Y是稀溶液,则三种酸浓度大小顺序是c(Z)>c(Y)>c(X),故B正确;
C.强电解质X完全电离,Y和Z部分电离,溶液浓度越大其电离程度越小,所以稀释前电离程度大小为X>Y>Z,故C正确;
D.根据B知,pH=2时,X和Y属于稀溶液,Z属于浓溶液,故D错误;
故选D.
【考点精析】关于本题考查的弱电解质在水溶液中的电离平衡,需要了解当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理才能得出正确答案.


科目:高中化学 来源: 题型:
【题目】4﹣甲基﹣2﹣乙基﹣1﹣戊烯经催化加成所得产物名称为( )
A.4﹣甲基一2一乙基戊烷
B.2,5﹣二甲基戊烷
C.2﹣乙基﹣4﹣甲基戊烷
D.2,4﹣二甲基己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列行为不符合安全要求的是
A. 将剩余的金属钠丢弃在废纸篓里
B. 少量酒精洒在桌子上着火时,立即用湿布扑灭
C. 闻气体时,用手轻轻扇动使少量气体飘进鼻孔
D. 稀释浓硫酸时,将浓硫酸沿器壁缓慢注入水中并不断搅拌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
A.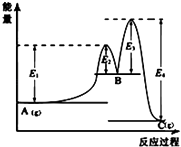
图中可以看出反应A(g)=C(g)的△H=(E1﹣E4)kJmol﹣1
B.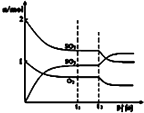
图中表示一定条件下进行的反应2SO2+O2═2SO3各成分的物质的量变化,t2时刻改变的条件可能是扩大了容器的体积
C.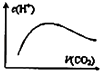
图中表示将CO2通入NaOH的稀溶液中,随着CO2的通入,溶液中水电离出的c(H+)变化关系
D.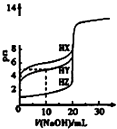
图中曲线表示用0.1000mol/L NaOH溶液分别滴定浓度相同的三种一元酸,由此可判断HX的酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用中和滴定法测定某盐酸的物质的量浓度。
(1)标准溶液应盛于___________(填“A”或“B”)滴定管中。
(2)若选用酚酞作指示剂,以0.1250 mol·L-1的标准氢氧化钠溶液滴定,如何判断滴定终点____________。
(3)实验数据记录如下表,请分析数据并计算,盐酸的物质的量浓度=_________mol·L-1。

滴定次数 | 待测溶液体积/mL | ||
标准碱液 | |||
滴定前读数/mL | 滴定后读数/mL | ||
1 | 20.00 | 0.00 | 16.02 |
2 | 20.00 | 0.00 | 15.98 |
3 | 20.00 | 0.00 | 16.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化及军事科学领域。所谓“纳米材料”是指研究开发出的直径从几纳米至几十纳米的材料。将纳米材料分散到空气中形成胶体,该胶体属于( )
A.固溶胶B.液溶胶C.气溶胶D.悬浊液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组探究少量Cl2和FeBr2反应的过程。
(1)配制FeBr2溶液:
ⅰ. 配制50mL1.0mol/LFeBr2溶液;
ⅱ. 上述溶液呈淡黄色。取少量此溶液,向其中滴入KSCN溶液,变为浅红色。
①配制50mL1.0mol/LFeBr2溶液常加少量HBr是为了_____________________。
②由ⅱ可知,此FeBr2溶液呈黄色的原因是其中含有________,用离子方程式解释产生其原因:_____________________。
(2)氯气和FeBr2反应实验操作及现象如下:

据此甲同学得出结论:少量Cl2既能和Fe2+又能和Br-发生氧化还原反应。
①Cl2和Fe2+发生反应的离子方程式是________________。
②乙同学认为上述实验不能证明Cl2和Br-发生反应,理由是_____________。
③乙同学改进实验如下:在上述FeBr2溶液中加入过量铁粉,取上层清液2 mL,向其中滴加3滴饱和氯水后,再加入CCl4,振荡后静置,观察现象。乙得出结论:少量Cl2只与Fe2+反应,不与Br-反应。乙得出该结论依据的实验现象是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com