
【题目】如图表示元素周期表前四周期的一部分,关于元素X、Y、Z、W的叙述正确的是( )

①X、Y的最高价氧化物的水化物酸性为Y<X;②Y、Z的气态氢化物的稳定性Y<Z;③W的单质常温下呈液态,一定条件下可与铁粉反应;④W的原子序数比Z大9。
A. 只有③ B. ①② C. ①②③ D. ①②③④
【答案】C
【解析】
试题由元素在周期表的位置可知,X为第二周期第ⅤA族元素,即X为N元素,则Y为P元素,Z为S元素,W为Br元素。①同一主族的元素,原子序数越大,元素的非金属性越弱,所以元素的非金属性X>Y,则最高价氧化物的含氧酸的酸性为Y<X,正确;②同一周期的元素,元素的原子序数越大,元素的非金属性越强,则元素的非金属性Z>Y,元素的非金属性越弱,其简单氢化物的稳定性就越强,所以气态氢化物的稳定性Y<Z,正确;③溴元素的单质Br2在常温下呈液体,由于具有强的氧化性,与变价金属铁反应生成溴化铁,正确;④Br的质子数为35,S的质子数为16,则W的原子序数比Z大35-16=19,错误;故上述说法正确的是①②③,选项C正确。


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
【题目】pH=1的某溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32﹣、SO32﹣、SO42﹣、Cl﹣、NO3﹣中的一种或几种(忽略水的电离及离子的水解),取该溶液进行连续实验,实验过程如图:下列有关推断不正确的是( )
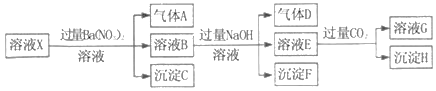
A. 溶液X中一定含有H+、Al3+、NH4+、Fe2+、SO42﹣
B. 根据上述连续实验不能确定溶液X中是否含有Fe3+、Cl﹣
C. 沉淀H为Al(OH)3、BaCO3的混合物
D. 若溶液X为100mL,产生的气体A为44.8mL(标准状况),则X中c(Fe2+)=0.06molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3、N2H4在工业生产和国防建设中都有广泛应用。回答下列问题:
(1)①N2H4 (g) ![]() N2(g)+2H2(g) △H1
N2(g)+2H2(g) △H1
②N2(g)+3H2(g) ![]() 2NH3(g) △H2
2NH3(g) △H2
③7N2H4(g) ![]() 8NH3(g)+3N2(g)+2H2(g) △H3
8NH3(g)+3N2(g)+2H2(g) △H3
△H3=___________(用含△H1和△H2的代数式表示)。
(2)纳米钴的催化作用下,N2H4可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝。当反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图所示。

该反应的△H________(填“>”或“<”)0,N2H4发生分解反应的化学方程式为___________。
(3)T℃时,向一体积为5L 的恒容密闭容器中充入总物质的量为2 mol的CO2和NH3,在一定条件下发生反应:2NH3(g)+CO2(g)====CO(NH2)2(s)+H2O(g)。混合气体中氨气的体积分数随反应时间的变化如图所示。

① 0~60s内,反应速率v(CO2)=________mol/(L·s)
② T℃时,该反应的化学平衡常数K=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.200mol·L-1NaOH溶液分别滴定20.0mL0.200 mol·L-1的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是

A. Ⅱ表示的是滴定醋酸的曲线
B. pH=7时,滴定醋酸消耗的V(NaOH)小于20mL
C. V(NaOH)=20.00mL时,两份溶液中c(Cl-)=c(CH3COO-)
D. V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>c(CH3COO-)> c(OH-)> c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氨水中存在电离平衡:NH3·H2O![]() NH4++OH-,下列情况能引起电离平衡向右移动的有( )
NH4++OH-,下列情况能引起电离平衡向右移动的有( )
①加NH4Cl固体 ②加NaOH溶液 ③通HCl ④加CH3COOH溶液 ⑤加水
A. ①③⑤ B. ①④⑤ C. ③④⑤ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4﹣O2燃料电池具有放电稳定,无污染等优点,如图为一用甲烷氧气燃料电池电解饱和氯化钠溶液的模型图。请认真读图,回答以下问题:

(1)请写出通入甲烷气体的一极所发生的电极反应式:____________________,其附近的pH值___(填“不变”或“变大”或“变小”)
(2)如果通入1mol的甲烷完全参与电极反应,则电路中转移_____________的电子,a电极产生的气体在标准状况下的体积为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关钠和镁的说法中正确的是( )
A.金属钠在氧气中燃烧可以生成氧化钠
B.金属钠在高温下能将TiCl4溶液中的钛置换出来
C.工业上用电解熔融氧化镁制取金属镁
D.金属镁燃烧后会发出耀眼的白光,因此常用来制造信号弹和焰火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(﹣NO2)还原为氨基(﹣NH2);在苯的溴代反应中用溴化铁作催化剂。
(1)N的原子结构示意图为_______,Fe基态原子核外电子排布式为_______。
(2)H、N、O 的电负性从小到大的顺序是_______。
(3)与NO2+互为等电子体的一种分子为_____(填化学式),氨基(﹣NH2)中氮原子的杂化类型为_____。
(4)1mol苯分子中含有σ键的物质的量为______。
(5)Fe 与 N 形成的某化合物晶胞如图所示,则该晶体的化学式为_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下图所示装置进行实验,并回答下列问题:

(1)锌极发生反应的电极反应式为_______________________________;铜极发生反应的电极反应式为_______________________________________________;
(2)石墨棒C1发生反应的电极反应式为____________________________;石墨棒C2附近发生的实验现象为____________________________________________。
(3)当C2极析出224 mL气体(标准状况)时,锌的质量减少_____g,CuSO4溶液的质量________(填“增加”或“减少”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com