
| A. | 25℃时,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12溶液.Na+、SO32一、ClO-、CO32- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、Fe2+、Cl-、NO3- | |
| C. | 0.1mol/LBa (OH)2溶液中:Al3+、NH4+、NO3-、HCO3- | |
| D. | 0.1mol/L AlO2-溶液中:Na+、K+、SO32一、CO32- |
分析 A.25℃时,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12溶液呈碱性,次氯酸根离子能够氧化亚硫酸根离子;
B.能与金属铝反应放出氢气的溶液中存在大量氢离子或氢氧根离子,亚铁离子与氢氧根离子反应,酸性条件下硝酸根离子能够氧化亚铁离子;
C.铝离子、铵根离子、碳酸氢根离子与氢氧化钡溶液反应;
D.四种离子之间不反应,都不与偏铝酸根离子反应.
解答 解:A.SO32-、ClO-之间发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.能与金属铝反应放出氢气的溶液中为酸性或强碱性溶液,Fe2+与碱性溶液中的氢氧根离子反应,Fe2+、NO3-在酸性条件下发生氧化还原反应,在溶液中一定不能大量共存,故B错误;
C.Al3+、NH4+、HCO3-与Ba (OH)2反应,在溶液中不能大量共存,故C错误;
D.Na+、K+、SO32-、CO32-之间不发生反应,都不与AlO2-反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.


科目:高中化学 来源: 题型:填空题
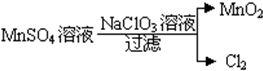
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
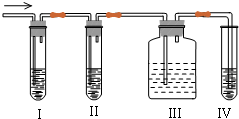
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
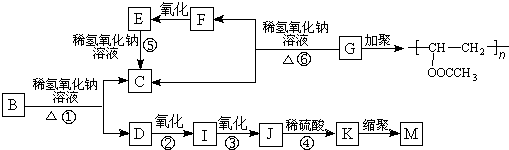
 .
.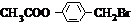 +3NaOH$→_{△}^{水}$CH3COONa+
+3NaOH$→_{△}^{水}$CH3COONa+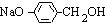 +NaBr+H2O,K与少量的氢氧化钠溶液反应:
+NaBr+H2O,K与少量的氢氧化钠溶液反应: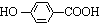 +NaOH→
+NaOH→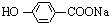 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z的氢化物的沸点是同主族元素中最高的 | |
| B. | 由X、Y、Z三种元素中的任意两种组成的具有10电子的微粒只有2种 | |
| C. | 仅由X、Y两种元素组成的化合物不止一种 | |
| D. | X和Z可以组成原子个数比分别为1:1和2:1常温下为液态的两种化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-乙基戊烷 | B. | 2-甲基-1-乙基苯 | ||
| C. | 2,4,4-三甲基己烷 | D. | 3-甲基-2-丁烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
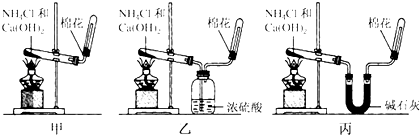
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
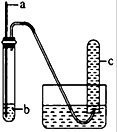 用如图装置进行实验,下列预期实验现象及相应结论均正确的是( )
用如图装置进行实验,下列预期实验现象及相应结论均正确的是( )| a | b | 预期实验 现象 | 结论 | |
| A | 铜丝 | 浓硝酸 | 试管c中有大量红棕色气体 | 硝酸有强氧化性 |
| B | 木条 | 18.4mol/L 硫酸 | 木条变黑 | 浓硫酸有酸性及 氧化性 |
| C | 生铁 | NaCl溶液 | 导管处发生倒吸 | 生铁发生吸氧腐蚀 |
| D | 铁丝 | 含少量HCl的H2O2溶液 | 试管c中有大量无色气体 | 该反应中铁作催化剂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁在潮湿的空气中易发生吸氧腐蚀生成Fe(OH)2,进一步被O2氧化为Fe(OH)3,Fe(OH)3脱去一部分水生成Fe2O3•nH2O,它就是铁锈的主要成分 | |
| B. | 分子筛中有许多笼状空穴和通道可用于分离、提纯气体,还可用作干燥剂、离子交换剂、催化剂和、催化剂载体 | |
| C. | 俄国化学家门捷列夫经过研究提出了元素周期律--元素性质随着元素原子量(相对原子质量)递增而呈周期性变化的规律,并列出第一张元素周期表 | |
| D. | 氧化铝陶瓷、硅藻土、沸石、立方氮化硼都是无机非金属材料,光导纤维、聚酯纤维、橡胶、酚醛树脂都是高分子材料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com