
【题目】下列实验设计能够成功的是 ( )
实验目的 | 实验步骤及现象 | |
A | 检验亚硫酸钠试样是否变质 | 试样 |
B | 检验某盐是否为铵盐 | 试样 |
C | 证明酸性条件下H2O2氧化性比I2强 | NaI溶液 |
D | 除去氯化钠晶体中少量硝酸钾 | 试样 |
A.AB.BC.CD.D
科目:高中化学 来源: 题型:
【题目】某化学小组用下列装置和试剂进行实验,探究O2与KI溶液发生反应的条件。
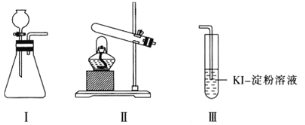
供选试剂:质量分数为30%的H2O2溶液、0.1 mol·L-1的H2SO4溶液、MnO2固体、KMnO4固体。
(1)小组同学设计甲、乙、丙三组实验,记录如下:
操作 | 现象 | |
甲 | 向装置I的锥形瓶中加入MnO2固体,向装置I的____中加入质量分数为30%的H2O2溶液,连接装置I、III,打开活塞 | 装置I中产生无色气体并伴随大量白雾;装置III中有气泡冒出,溶液迅速变蓝 |
乙 | 向装置II中加入KMnO4固体,连接装置II、III,点燃酒精灯 | 装置III中有气泡冒出,溶液不变蓝 |
丙 | 向装置II中加入____,向装置III中再加入适量0.1mol·L-1的H2SO4溶液,连接装置II、III,点燃酒精灯 | 装置III中有气泡冒出,溶液变蓝 |
(2)丙实验中O2与KI溶液反应的离子方程式为___________________________________。
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是__________。为进一步探究该条件对反应速率的影响,可采取的实验措施是____________________________。
(4)由甲、乙、丙三组实验推测,甲实验中可能是I中的白雾使溶液变蓝。为了验证推测,可将装置I中产生的气体通入_________(填字母)溶液中,依据实验现象来证明白雾中含有H2O2。
A.酸性KMnO4 B.FeCl2 C.H2S
(5)资料显示:KI溶液在空气中久置的过程中会被缓慢氧化:4KI+O2+2H2O=2I2+4KOH。该小组同学取20 mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应___________________________________(写离子方程式)造成的,请设计实验证明他们的猜想是否正确:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚又称甲醚,简称DME,熔点![]() ,沸点
,沸点![]() ,与石油液化气
,与石油液化气![]() 相似,被誉为“21世纪的清洁燃料”。制备原理如下:
相似,被誉为“21世纪的清洁燃料”。制备原理如下:
(I)由天然气催化制备二甲醚:①![]() ;
;
(II)由合成气制备二甲醚:
②![]() ;
;
③![]() 。
。
回答下列问题:
(1)若甲烷和二甲醚的燃烧热分别是![]() 和
和![]() ;
;![]() 液态水变为气态水要吸收
液态水变为气态水要吸收![]() 的热量。则
的热量。则![]() ________
________![]() 。
。
(2)反应③的化学平衡常数表达式为![]() ________。制备原理Ⅰ中,在恒温、恒容的密闭容器中合成,将气体按
________。制备原理Ⅰ中,在恒温、恒容的密闭容器中合成,将气体按![]() 混合,图中能正确反映反应①中
混合,图中能正确反映反应①中![]() 的平衡体积分数随温度变化的曲线是________。下列能表明反应①达到化学平衡状态的是________
的平衡体积分数随温度变化的曲线是________。下列能表明反应①达到化学平衡状态的是________![]() 填字母
填字母![]() 。
。
A.混合气体的密度不变
B.反应容器中二甲醚的百分含量不变
C.反应物的反应速率与生成物的反应速率之比等于化学计量数之比
D.混合气体的压强不变

(3)有人模拟制备原理Ⅱ,在500K时的2L的密闭容器中充入2molCO和![]() ,此时体系总压强是
,此时体系总压强是![]() 。8min达到平衡,平衡时CO浓度为
。8min达到平衡,平衡时CO浓度为![]() ,
,![]() ,则CO的转化率为________,用平衡分压表示可逆反应③的平衡常数
,则CO的转化率为________,用平衡分压表示可逆反应③的平衡常数![]() ________
________![]() 分压
分压![]() 总压
总压![]() 物质的量分数
物质的量分数![]() 。
。
(4)在500K时的2L的密闭容器中充入![]() ,发生反应③,容器的总压强为4000kPa,反应5min后达到平衡,
,发生反应③,容器的总压强为4000kPa,反应5min后达到平衡,![]() ,用单位时间甲醇的分压变化表示该反应的反应速率为________。
,用单位时间甲醇的分压变化表示该反应的反应速率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列图示的说法中,正确的是:
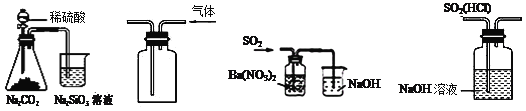
① ② ③ ④
A.图①所示实验可比较硫、碳、硅三种元素的非金属性强弱
B.用图②所示实验装置排空气法收集CO2气体
C.用图③所示实验装置制备BaSO3沉淀
D.图④装置可以用来除去SO2中的HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
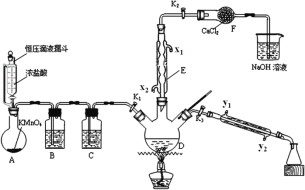
【题目】如图是某小组设计的用干燥氯气和甲苯合成一氯化苄(C6H5CH2Cl,其中C6H5-表示苯基)并分离产物的实验装置。甲苯及各种氯化苄的物理性质如表所示。
物理性质 | 熔点℃ | 沸点℃ | 密度gcm-3 |
甲苯 | -95 | 110 | 0.86 |
一氯化苄(C6H5CH2Cl) | -45 | 179 | 1.10 |
二氯化苄(C6H5CHCl2) | -17 | 205 | 1.26 |
三氯化苄(C6H5CCl3) | -4.4 | 221 | 1.37 |
回答下列问题:
(1)仪器F的名称是__________;
(2)瓶B和C中盛放的试剂应分别为__________(填序号);
a.蒸馏水;浓硫酸 b.饱和食盐水;浓硫酸
c.浓硫酸;酸性KMnO4溶液 d.饱和NaHCO3溶液;浓硫酸
(3)两处冷凝水的进水口应分别为__________(填序号);
A . x1、y1 B. x1、y2 C. x2、y1 D.x2、y2
(4)在回流反应的过程中,由于温度控制不当,部分产物从K2处被蒸出。取烧杯中的少量吸收液于试管中,滴入新制氢氧化铜悬浊液并加热,观察到有砖红色沉淀生成。则在吸收液中发生反应的化学方程式为______________________;
(5)反应结束后,撤去E、F及尾气吸收装置,插上玻璃塞。保持K1关闭,打开K3,加热三颈烧瓶,分馏出一氯化苄,应选择的温度范围是__________;
(6)由于某同学操作时不慎将含铁的沸石加入三颈烧瓶,在分馏时得到了异常馏分X。用质谱法测得X的相对分子质量与二氯化苄相同,核磁共振氢谱显示X中有3种不同化学环境的氢。已知苯环上存在甲基或氯甲基是,后续取代苯环的基团主要引入其邻位或对位,X的结构简式可能为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条作下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g) ![]() 2SO3(g) △H<0。查阅资料知SO3的熔点为16.83℃,沸点是448℃。某化学学习小组欲通过实验测定上述反应中SO2的转化率,他们设计了如下实验。
2SO3(g) △H<0。查阅资料知SO3的熔点为16.83℃,沸点是448℃。某化学学习小组欲通过实验测定上述反应中SO2的转化率,他们设计了如下实验。
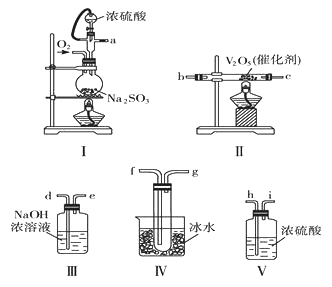
请根据要求回答问题:
(1)各装置接口的连接顺序是a→_________________。
(2)装置Ⅳ烧杯中盛放冰水的作用是_____________________。
(3)装置Ⅰ所用硫酸,一般选用浓度为70%~80%的硫酸,原因是_________________。
(4)当装置Ⅰ中反应结束时,要打开止水夹继续通入O2一段时间,继续通入O2的目的是_______。
(5)称量agNa2SO3粉末与足量硫酸反应,实验结束后称得装置Ⅳ增重bg,列式表示该实验中SO2的转化率__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员研制出一种室温“可呼吸”Na-CO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。吸入CO2时,其工作原理如右图所示。吸收的全部CO2中,有![]() 转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法正确的是( )
转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法正确的是( )

A. “吸入”CO2时,钠箔为正极
B. “吸入”CO2时的正极反应:4Na++ 3CO2+ 4e-= 2Na2CO3+ C
C. “呼出”CO2时,Na+向多壁碳纳米管电极移动
D. 标准状况下,每“呼出”22.4 L CO2,转移电子数为0.75 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化磷(PCl3)是一种重要的有机合成催化剂。实验室常用红磷与干燥的Cl2制取PCl3,装置如图所示。

已知: PCl3熔点为-112℃,沸点为75.5℃。易被氧化,遇水易水解。与Cl2反应生成PCl5。
(1)A中反应的化学方程式为__________________。
(2)B中所装试剂名称是___________________,E中碱石灰的作用是___________________。
(3)实验时,检查装置气密性后,向C装置的曲颈甑中加入红磷,打开止水夹K通入干燥的CO2,一段时间后,关闭K,加热曲颈甑至上部有黄色升华物出现时通入氯气,反应立即进行。通干燥CO2的作用是____________________。CO2______(选填“能”或“不能”)用Cl2代替,理由是________________。
(4)D中烧杯中盛装__________,其作用是_______________。
(5)PCl3水解得到亚磷酸(分子式:H3PO3。二元弱酸),写出亚磷酸钠被浓硝酸氧化的离子方程式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积相同的两个密闭容器M和N中,保持温度为150 ℃,向M容器中加入a mol HI,同时向N容器中加入b mol HI (a>b)。当反应2HI(g)![]() H2 (g) + I2 (g) 达到平衡后,下列说法正确的是
H2 (g) + I2 (g) 达到平衡后,下列说法正确的是
A.从反应开始到达到平衡,所需时间tM > tN
B.平衡时cM(I2) = c N(I2)
C.平衡时I2 蒸气在混合气体中的体积分数:M > N
D.HI的平衡分解率αM = αN
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com