
【题目】一定温度下的密闭容器中存在如下反应:CO(g)+ H2O(g)![]() CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2 molL-1,经测定该反应在该温度下的平衡常数K=1,试判断:
CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2 molL-1,经测定该反应在该温度下的平衡常数K=1,试判断:
(1)当CO转化率为25%时,该反应是否达到平衡,若未达到,向哪个方向进行?
(2)当CO的起始浓度仍为2 molL﹣1,H2O(g)的起始浓度为6 molL﹣1,求平衡时CO的转化率?
【答案】(1)不是平衡状态,会向正方向进行
(2)平衡时CO的转化率为75%
【解析】
试题分析:(1) CO(g) + H2O(g) ![]() CO2(g) + H2(g)
CO2(g) + H2(g)
起始浓度(molL1) 2 2 0 0
转化浓度(molL1) 0.5 0.5 0.5 0.5
平衡浓度(molL1) 1.5 1.5 0.5 0.5
则Q=0.5×0.5÷(1.5×1.5)=1/9<K,反应未达到平衡,向正反应方向移动。
(2)设达到平衡时,CO转化浓度为y,则
CO(g) + H2O(g) ![]() CO2(g) + H2(g)
CO2(g) + H2(g)
起始浓度(mol/L) 2 6 0 0
转化浓度(mol/L) y y y y
平衡浓度(mol/L) 2-y 6-y y y
![]() ,解得y=1.5mol·L-1,α(CO)= 1.5mol·L-1÷2molL1×100%=75%。
,解得y=1.5mol·L-1,α(CO)= 1.5mol·L-1÷2molL1×100%=75%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、W为五种短周期元素。X原子的质子数与电子层数相同,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示。下列说法不正确的是( )
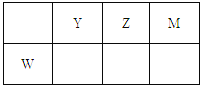
A. 原子半径:W>Y>Z>M>X
B. 热稳定性:XM>X2Z,沸点:X2Z>YX3
C. X、Y、Z三种元素形成的化合物中不可能含离子键
D. YM3、WM4分子中每个原子最外层均满足8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是 ( )
A. 电解氯化镁溶液:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B. 氢氧化铁与足量的氢溴酸溶液反应:Fe(OH)3+3H+=Fe3++3H2O
C. 氢氧化钡溶液中加入硫酸:Ba2++OH—+H++SO42—=BaSO4↓+H2O
D. 鸡蛋壳浸泡在盐酸中产生气泡:CO32—+2H+=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分氧化的FeCu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理:下列说法正确的是( )
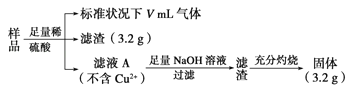
A.滤液A中的阳离子为Fe2+、Fe3+、H+
B.样品中CuO的质量为4.0g
C.V=448
D.原样品中Fe元素的质量分数为41%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于任何一个平衡体系,采用以下措施,一定会使平衡移动的是( )
A. 加入一种反应物 B. 升高温度
C. 对平衡体系增加压强 D. 使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为:2KClO3+4HCl(浓)===2KCl+2ClO2↑+Cl2↑+2H2O。
(1)请分析该反应中电子转移的情况(单线桥法表示):__________________。
(2)浓盐酸在反应中显示出来的性质是________。(填写编号)
①只有还原性;②还原性和酸性;③只有氧化性;④氧化性和酸性。
(3)产生0.1 mol Cl2,则转移的电子的物质的量为________mol。
(4)ClO2具有很强的氧化性。因此,常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是Cl2的________倍。(ClO2 Cl2还原产物为Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于吸热反应的说法,正确的是( )
A. 凡需加热的反应一定是吸热反应 B. 只有分解反应才是吸热反应
C. 使用催化剂的反应是吸热反应 D. 酸碱中和反应的逆反应是吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com