
【题目】部分氧化的FeCu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理:下列说法正确的是( )
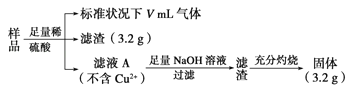
A.滤液A中的阳离子为Fe2+、Fe3+、H+
B.样品中CuO的质量为4.0g
C.V=448
D.原样品中Fe元素的质量分数为41%
【答案】C
【解析】
试题分析:硫酸足量、滤液A不含Cu2+,可知加入硫酸后的3.2g滤渣全是铜;加入氢氧化钠后的滤渣、灼烧后得固体是氧化铁共3.2g。所以原合金中铜元素3.2g、铁元素![]() ;合金样品氧元素的质量是5.76g-3.2g-2.24g=0.32g。有铜析出,所以滤液中不可能含有Fe3+,故A错误;铜元素+氧元素=3.52g,,所以CuO的质量不可能为4.0g,故B错误;反应后生成硫酸亚铁的物质的量是
;合金样品氧元素的质量是5.76g-3.2g-2.24g=0.32g。有铜析出,所以滤液中不可能含有Fe3+,故A错误;铜元素+氧元素=3.52g,,所以CuO的质量不可能为4.0g,故B错误;反应后生成硫酸亚铁的物质的量是![]() 0.04mol;所以参加反应的硫酸0.04mol,反应生成水
0.04mol;所以参加反应的硫酸0.04mol,反应生成水![]() 0.02mol;所以生成氢气0.04mol-0.02mol=0.02mol,标准状况下的体积是448mL,故C正确;原样品中Fe元素的质量分数为
0.02mol;所以生成氢气0.04mol-0.02mol=0.02mol,标准状况下的体积是448mL,故C正确;原样品中Fe元素的质量分数为![]() 38.9%,故D错误。
38.9%,故D错误。


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】常温下,用浓度为0.1000mol·L-1的NaOH溶液分别逐滴加入到20.00mL 0.1000mol·L-1的HX、HY溶液中,pH随NaOH溶液体积的变化如图。下列说法正确 ( )
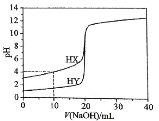
A.V(NaOH)=10.00 mL时,c(X-)>c(Na+)>c(H+)>c(OH-)
B.V(NaOH)=20.00 mL时,两份溶液中,c(X-)>c(Y-)
C.V(NaOH)=20.00 mL时,c(Na+) > c(X-) >c(OH-)>c(H+)
D.pH=7时,两份溶液中,c(X-)=c(Y-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达到平衡,平衡常数K = c(CO)c(H2O)/c(CO2)c(H2),恒容时,温度升高,H2浓度减小。下列说法正确的是
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的化学方程式为CO+H2O ![]() CO2+H2
CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池总反应的离子方程式为2Fe3++Fe===3Fe2+,不能实现该反应的原电池是
A. 正极为Cu,负极为Fe,电解质溶液为FeCl3
B. 正极为C,负极为Fe,电解质溶液为Fe(NO3)3
C. 正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3
D. 正极为Ag,负极为Fe,电解质溶液为Fe2(SO4)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下的密闭容器中存在如下反应:CO(g)+ H2O(g)![]() CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2 molL-1,经测定该反应在该温度下的平衡常数K=1,试判断:
CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2 molL-1,经测定该反应在该温度下的平衡常数K=1,试判断:
(1)当CO转化率为25%时,该反应是否达到平衡,若未达到,向哪个方向进行?
(2)当CO的起始浓度仍为2 molL﹣1,H2O(g)的起始浓度为6 molL﹣1,求平衡时CO的转化率?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法完全正确的是
A. 有机化合物都是非电解质 B. 有机化合物都不能溶于水
C. 有机化合物都能燃烧 D. 有机化合物都含有碳元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1moLSO2和1moLO2通入固定容积密闭容器中,在一定条件下反应达到平衡,平衡时SO3为0.2moL,此时若移去0.5moLSO2和0.5moLO2,在同一温度下反应达到新的平衡时,SO3的物质的量是( )
A.0.2moL B.0.1moL
C.小于0.1moL D.大于0.1moL,小于0.2moL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com