
【题目】反应A(g)+B(g) ![]() 2C(g)+3D(g)在四种不同情况下的反应速率如下,其中表示
2C(g)+3D(g)在四种不同情况下的反应速率如下,其中表示
反应速率最快的是
A. v(A)=0.20mol·L-1·min-1 B. v(B)=0.30 mol·L-1·min-1
C. v(C)=0.40 mol·L-1·min-1 D. v(D)=0.50 mol·L-1·min-1
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】常温下,向10.00 mL 0.1mol/L某二元酸H2X溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化如图所示(忽略温度变化),已知:常温下,H2X的电离常数Ka1 = 1.1×10-5 ,Ka2 = 1.3×10-8。下列叙述正确的是( )
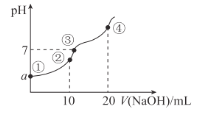
A.从点①到点④过程中水的电离程度先增大后减小
B.点②处c(Na+) + 2c(H+) + c(H2X) =2 c(X2-) + c(HX-) + 2c(OH-)
C.a近似等于3
D.点④处c(Na+) = 2 c(X2-) > c(OH-) > c(HX-) > c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为________,中心原子的杂化方式为__________________。
(2)As4O6的分子结构如图所示,其中As原子的杂化方式为______________。
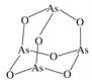
(3)AlH4-中,Al原子的轨道杂化方式为__________;列举与AlH4-空间构型相同的一种离子和一种分子:__________、__________(填化学式)。
(4)用价层电子对互斥理论推断SnBr2分子中,Sn原子的轨道杂化方式为____________,SnBr2分子中Br-Sn-Br的键角________120°(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能得出相应结论的是
选项 | 实验操作或现象 | 实验结论 |
A | 在含 NaOH 的 Mg(OH)2 悬浊液中滴加 CoCl2 溶液,产生粉红色沉淀 | Ksp[Co(OH)2]<Ksp[Mg(OH)2] |
B | 在透明溶液中通入 CO2,产生白色胶状沉淀 | 原溶液中一定含有 SiO32- |
C | 在新制氯水中加入碳酸钙粉末,搅拌,过滤 | 氯水的漂白性会增强 |
D | 将 Fe 粉、Cu 粉分别与硫粉混合加热,分别生成 FeS、Cu2S | 还原性:Fe>Cu |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)卤族元素位于元素周期表的__________________区;溴的价电子排布式为______________________。
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2 形式存在的。使氢氟酸分子缔合的作用力是____________________。
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是____________________(写出 名称)。
氟 | 氯 | 溴 | 碘 | |
第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图 a、b 所示:
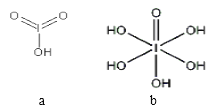
请比较二者酸性强弱:HIO3______________________H5IO6(填“>”、 “<”或“=”)。
(5)已知 ClO2-为 V 形,中心氯原子周围有四对价层电子。 ClO2-中心氯原子的杂化轨道类型为___________________,写 出一个 ClO2-的等电子体______________________。
(6)如图为碘晶体晶胞结构。有关说法中正确的是______________________。
A.碘分子的排列有 2 种不同的取向,2 种取向不同的碘分子 以 4 配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有 4 个碘原子
C.碘晶体中微粒(碘分子)的堆积为最密堆积
D.碘晶体中存在的相互作用有非极性键和范德华力
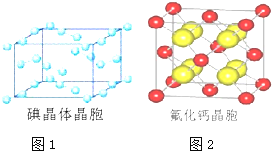
(7)已知 CaF2 晶体(见图)的密度为ρg/cm3,NA 为阿伏加德罗常数,棱上相邻的两个 Ca2+ 的核间距为 a cm, 则 CaF2 的相对分子质量可以表示为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语错误的是( )
A.稀盐酸溶液与稀氢氧化钠的中和热:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ· mol-1
B.FeCl3溶液水解的离子方程式:Fe3++3H2O![]() Fe (OH)3+3H+
Fe (OH)3+3H+
C.热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ·mol-1,一定条件下,将0.5mol N2(g)和1.5molH2(g)置于密闭的容器中反应生成NH3(g),则放热19.3kJ
2NH3(g) △H=-38.6kJ·mol-1,一定条件下,将0.5mol N2(g)和1.5molH2(g)置于密闭的容器中反应生成NH3(g),则放热19.3kJ
D.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g)=2CO(g)+O2(g) ΔH=+566.0 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在家中进行化学实验,按照图A连接好线路发现灯泡不亮,按照图B连接好线路发现灯泡亮.
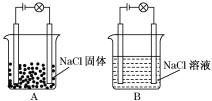
依据上述现象判断或回答下列问题:
(1)NaCl属于________(“酸”、“碱”或“盐”),因为__________________________.
(2)NaCl固体________(填“能”或“不能”)导电,原因是_____________________.
(3)NaCl溶液________(填“能”或“不能”)导电,原因是__________________.
(4)在NaCl固体、NaCl溶液中属于电解质的是_________________________________,
原因是____________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有室温下四种溶液,下列有关叙述不正确的是( )

A. ③和④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大
B. ②和③两溶液等体积混合,所得溶液中c(H+)>c(OH-)
C. 分别加水稀释10倍,四种溶液的pH:①>②>④>③
D. V1L ④与V2L ①溶液混合后,若混合后溶液pH=7,则V1<V2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元弱酸H2A溶液,按下式发生电离:H2A![]() H++HA-、HA-
H++HA-、HA-![]() H++A2-,下列四种溶液中c(A2-)最大的是( )
H++A2-,下列四种溶液中c(A2-)最大的是( )
A.0.01 mol·L-1的H2A溶液
B.0.01 mol·L-1的NaHA溶液
C.0.02 mol·L-1的盐酸与0.04 mol·L-1的NaHA溶液等体积混合液
D.0.02 mol·L-1的NaOH与0.02 mol·L-1的NaHA溶液等体积混合液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com