
亚铁盐中,FeSO4?7H2O露置于空气中易被氧气氧化,而莫尔盐[(NH4)2SO4?FeSO4?6H2O]露置于空气中不易被氧气氧化,是一种重要的定量分析试剂。其制备原理是:FeSO4+(NH4)2SO4+6H2O =(NH4)2SO4?FeSO4?6H2O。
实验室用废铁屑制备莫尔盐的过程如下:
(1)步骤I除锈的操作是:将废铁屑放入烧杯, ,过滤,洗涤。
(2)步骤II铁屑的溶解在锥形瓶中进行,并水浴加热到60℃左右,需要的仪器是铁架台、石棉网、大烧杯、 。
(3)步骤III中加入的(NH4)2SO4与溶液中FeSO4的物质的量需满足的关系为:n[(NH4)2SO4]∶n[FeSO4]= 。
为了确定(NH4)2SO4的用量,下列方法简便可行的是 (填编号)。
A.称量废铁屑的质量,推算所需(NH4)2SO4的质量
B.称量无锈铁屑和步骤II之后剩余铁屑的质量,推算所需(NH4)2SO4的质量
C.测定FeSO4溶液的浓度和体积,推算所需(NH4)2SO4的质量
(4)所得晶体样品中可能混有的杂质是FeSO4·7H2O和(NH4)2SO4中的一种。某小组设计了如下方案进行检验和测定,请在答题卡上完成表中内容。
| 序号 | 实验方案 | 实验现象和结论 |
| 步骤1 | 取少量样品 | 样品颜色可能有变化。 |
| 步骤2 | 步骤1后将样品转移到试管中,加入去氧蒸馏水,振荡溶解,调节至酸性,________ ___________ __ 。 | 若 ,说明样品中含有FeSO4·7H2O杂质。 |
| 步骤3 | 若步骤2证明样品不含FeSO4?7H2O杂质,再另取样品测定其中NH4+的质量分数w1与理论值w2比较。 | 若w1 w2,说明样品中含有(NH4)2SO4杂质。 |
(16分)
(1)加入足量稀硫酸(或稀盐酸),充分搅拌 (2分)
(2)酒精灯、温度计 (4分,每空2分)
(3)1∶1 B (4分,每空2分)
(4)(6分,每空2分)序号 实验方案 实验现象和结论 步骤1 取少量样品 露置空气一段时间(1分) 样品颜色可能有变化。 步骤2 步骤1后将样品转移到试管中,加入去氧蒸馏水,振荡溶解,调节至酸性,_加入1~2滴KSCN溶液(2分)__ 若溶液变成血红色(2分),说明样品中含有FeSO4·7H2O杂质。 步骤3 若步骤2证明样品不含FeSO4 ·7H2O杂质,再另取样品测定其中NH4+的质量分数w1与理论值w2比较。 若w1 >(或大于)(1分)w2,说明样品中含有(NH4)2SO4杂质。
解析试题分析:(1)废铁屑含有单质铁和铁锈,铁锈主要成分是氧化铁,氧化铁是碱性氧化物,易溶于强酸,生成盐和水,因此步骤I除锈的操作是:将废铁屑放入烧杯,加入足量稀硫酸(或稀盐酸),充分搅拌,过滤,洗涤;(2)水浴加热装置需要的仪器是铁架台、石棉网、大烧杯、酒精灯、温度计;(3)步骤III的原理为FeSO4+(NH4)2SO4+6H2O =(NH4)2SO4?FeSO4?6H2O,该反应中n[(NH4)2SO4]∶n[FeSO4]=1∶1;A项,称取废铁屑的质量,不能推断硫酸铵的量,因此废铁屑中铁锈与单质铁的组成比例未知,过量的无锈铁屑的量未知,不能确定硫酸亚铁的量,故A选项错误;B项,称量无锈铁屑和步骤II之后剩余铁屑的质量,可以计算出与稀硫酸反应时消耗单质铁的量,根据硫酸亚铁与消耗单质铁的系数之比可以求生成的硫酸亚铁的量,进而推算所需(NH4)2SO4的质量,故B选项正确;C项,测定FeSO4溶液的浓度和体积,可以求硫酸亚铁的量,进而推算所需(NH4)2SO4的质量,但是需要进行滴定实验,配制标准酸性高锰酸钾溶液,因此不简便可行,故C选项错误;(4)硫酸铵是白色固体,七水合硫酸亚铁(或绿矾)是绿色固体,在空气中露置时,前者不易变质,而后者则容易被空气中的氧气氧化为铁盐,铁盐固体为黄色,因此样品露置之后颜色可能有变化;硫酸铁、硫酸亚铁都易溶于水,步骤1所得固体用去氧蒸馏水溶解,目的是防止蒸馏水中溶解的氧气氧化亚铁离子,调节至酸性后,加入KSCN溶液,溶液变为血红色,说明存在铁离子,证明样品中含有含有FeSO4·7H2O杂质;摩尔盐或(NH4)2SO4?FeSO4?6H2O中NH4+的质量分数计算表达式为: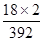 ×100%=9.18%,而(NH4)2SO4中NH4+的质量分数计算表达式为:w2=
×100%=9.18%,而(NH4)2SO4中NH4+的质量分数计算表达式为:w2=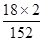 ×100%=23.68%,因此理论值w2=9.18%,若含有(NH4)2SO4时,w1介于二者9.18%与23.68%之间,所以w1> w2时,说明摩尔盐中含有硫酸铵杂质。
×100%=23.68%,因此理论值w2=9.18%,若含有(NH4)2SO4时,w1介于二者9.18%与23.68%之间,所以w1> w2时,说明摩尔盐中含有硫酸铵杂质。
考点:考查化学实验方案的设计与评价,涉及除去废铁屑中铁锈的实验操作、水浴加热装置所用仪器、物质的量在化学方程式计算中的应用、实验方案的评价、摩尔盐中杂质成分探究实验方案的设计、包括亚铁离子的氧化、铁离子的显色反应、铵根离子质量分数测定理论值与实际值大小关系等。


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:实验题
以废铁屑为原料制备FeCl3溶液,用作印刷电路铜板腐蚀剂,并对溶液B进行电解处理的实验流程如下: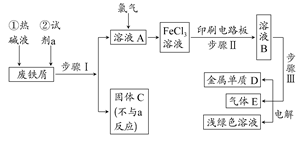
(1)试剂a应选用 (填写名称);
(2)步骤I用到的主要玻璃仪器有漏斗、 (填写仪器名称);
(3)写出步骤Ⅱ中主要反应的化学方程式: ;
(4)实验室制取气体E的离子方程式是 ,欲对气体E进行干燥和吸收,需选用下列装置中的 (填写序号);
(5)如何用化学方法检验气体E? 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
主要用于煤矿井下急救。某兴趣小组拟选用如下装置制备超氧化钾(部分夹持仪器已略去)。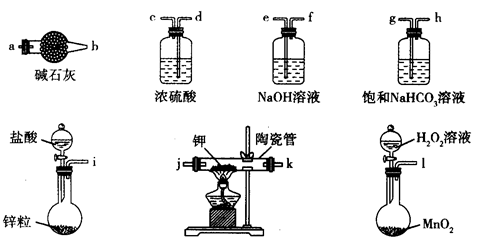
请回答下列问题:
(1)请选择必要的装置,按气流方向的连接顺序为_____________(填仪器接口的字母)。
(2)请根据完整的实验装置,完成下列实验步骤:①_____________________;②装入药品,打开分液漏斗活塞;③持续通入气体一段时间后,点燃酒精灯进行反应;④反应结束后,熄灭酒精灯,待反应管冷却至室温,停止通入氧气,并关闭分液漏斗的活塞;⑤拆除装置,取出产物。
(3)数据记录如下:
根据数据计算可得实验式KOx,则x=____________________。
(4)超氧化钾可吸收二氧化碳,并生成氧气,因此可以作为飞船、潜艇等密闭系统的氧气再生剂。写出超氧化钾与二氧化碳反应的化学方程式:__________________________。与过氧化钠相比,其优点是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
自来水生产的流程示意图见下:
(1)混凝剂除去悬浮物质的过程 (填写序号)
①只是物理变化 ②只是化学变化 ③是物理和化学变化
FeSO4·7H2O是常用的混凝剂,它在水中最终生成 沉淀。
(2)实验室过滤操作所用到的玻璃仪器是 。
(3)我们有时感觉自来水“有漂白粉气味”是因为使用了氯气消毒,请写出有关的化学反应方程式 。
下列物质中, 可以作为氯气的代用品。(填写序号)
① 臭氧 ②NH3(液) ③K2FeO4 ④SO2
(4)有些地区的天然水中含有较多的钙、镁离子。用离子交换树脂软化硬水时,先后把水通过分别装有离子交换树脂和 离子交换树脂的离子交换柱。(填“阴”或“阳”)
(5)测定水中的溶解氧:量取20mL水样,迅速加入MnSO4和KOH混合溶液,再加入KI溶液,立即塞好塞子,振荡使完全反应。打开塞子,迅速加入适量硫酸溶液,此时有碘单质生成。用0.10mol/LNa2S2O3溶液滴定生成的碘,消耗了6.00mL Na2S2O3溶液。已知在碱性溶液中,氧气能迅速氧化Mn2+,生成物在酸性条件下可以将碘离子氧化为碘单质,本身重新还原为Mn2+。
上述过程发生的反应可表示为:2Mn2++4OH-+O2=2MnO(OH)2
MnO(OH)2+2I-+4H+=I2+Mn2++3H2O I2+2S2O32-=2I-+S4O62-
求水中的溶解氧量(以mg·g-1为单位)
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
下图所示为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去),请根据要求完成下列各题(仪器装置可任意选用,必要时可重复选择,a、b为活塞)。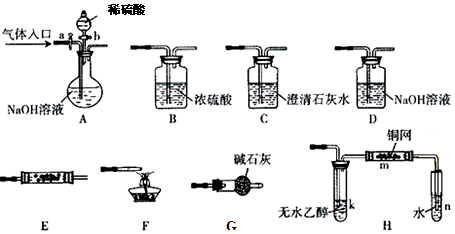
(1)若气体入口通入CO和CO2的混合气体,E内放置CuO,选择装置获得纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为 (填代号)。能验证CO氧化产物的现象是 。
(2)停止CO和CO2混合气体的通入,E内放置Na2O2,按A→E→D→B→H装置顺序制取纯净干燥的O2,并用O2氧化乙醇。此时,活塞a应 ,活塞b应 ,需要加热的仪器装置有 (填代号),m中反应的化学方程式为: 。
(3)若气体入口改通空气,分液漏斗内改加浓氨水,圆底烧瓶内改加NaOH固体,E内放置铂铑合金网,按A→G→E→D装置顺序制取干燥的氨气,并验证氨的某些性质。
①装置A中能产生氨气的原因有 。
②实验中观察到E内有红棕色气体出现,证明氨气具有 性。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
NiSO4?6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有:Cu、Zn、Fe、Cr等元素的化合物杂质)为原料获得。有关工艺流程如下: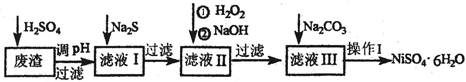
(1)往废渣中加H2SO4酸漫,要充分搅拌,其目的是 。
(2)加Na2S的目的是除去铜、锌等杂质,请写出除去Cu2+的离子方程式 。
(3)加6%的H2O2时,温度不能过高,其目的是 。
(4)除铁方法:用H2O2充分氧化后,再用NaOH控制pH值2~4范围内生成氢氧化铁沉淀。在上述方法中,氧化剂可用NaClO3代替,用NaClO3氧化Fe2+的离子方程式为 。
(5)上述流程中滤液III的溶质的主要成分是: 。
(6)操作I包括以下过程:过滤,用H2SO4溶解, 、 、过滤、洗涤获得产品。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验室制备1,2-二溴乙烷的反应原理如下:
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。
用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示: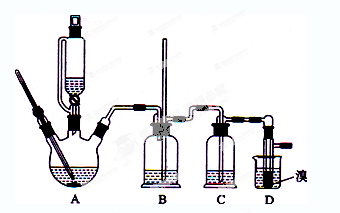
有关数据列表如下:
| | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验方案设计中,可行的是
| A.用萃取的方法可将汽油和煤油进行分离 |
| B.加过量稀盐酸后过滤,可除去混在铜粉中的少量镁粉和铝粉 |
| C.用溶解、过滤的方法可分离硝酸钾和氯化钠固体混合物 |
| D.将混有氢气的氧气通过灼热的氧化铜,以除去其中的氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各实验装置图的叙述中,正确的是( )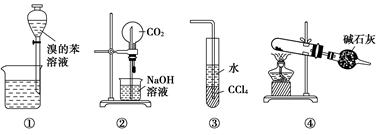
| A.装置①为放出萃取溴水后的苯层 |
| B.装置②为喷泉实验 |
| C.装置③可用来吸收HCl气体 |
| D.以NH4Cl为原料,装置④可用于制备少量NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com