
【题目】在一定温度下,向aL密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(s)+2Y(g)2Z(g),能判断该反应达平衡状态的是( )
A.容器内气体压强不随时间变化
B.容器内气体密度不随时间变化
C.容器内X,Y,Z的浓度之比为1:2:2
D.X的消耗速率和Z的生成速率之比为1:2
【答案】B
【解析】解:A.反应前后的气体的化学计量数之和相等,容器内的压强是个定值,始终不变,所以不能确定达到平衡,故A错误;
B.依据ρ= ![]() ,容器的体积不变,即V不变,而混合气体的质量随着反应方向不同始终变化,所以则ρ在未达到平衡前始终变化,当ρ不变时,可以说明反应达到平衡,故B正确;
,容器的体积不变,即V不变,而混合气体的质量随着反应方向不同始终变化,所以则ρ在未达到平衡前始终变化,当ρ不变时,可以说明反应达到平衡,故B正确;
C.容器内X、Y、Z的浓度之比为1:2:2,不能确定各物质的浓度不变,不能确定是否达到平衡状态,故C错误;
D.X的消耗速率和Z的生成速率都代表正方向速率,不能确定V(正)与V(逆)是否相等,所以不能确定是否达到平衡状态,故D错误;
故选:B.
【考点精析】本题主要考查了化学平衡状态的判断的相关知识点,需要掌握状态判断:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不变④若A、B、C、D为气体,且m+n≠x+y,压强恒定⑤体系颜色不变⑥单位时间内某物质内化学键的断裂量等于形成量⑦体系平均式量恒定(m+n ≠ x+y)等才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)2SO3(g)△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的( ) 
A.图Ⅰ研究的是t0时刻增大O2的物质的量浓度对反应速率的影响
B.图Ⅱ研究的是t0时刻通入氦气增大体系压强对反应速率的影响
C.图Ⅲ研究的是催化剂对化学平衡的影响,且甲的催化效率比乙高
D.图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A. 燃烧、酸碱中和反应都是放热反应
B. 化学反应必然伴随着能量的变化
C. 吸热反应中断键所需能量总和小于成键放出能量总和
D. 反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把100mL0.3mol/L的硫酸溶液和50mL0.6mol/L的硫酸溶液充分混合后,该溶液中H+的物质的量浓度为
A. 0.6mol/L B. 0.8mol/L C. 0.3mol/L D. 0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”.以钛铁矿(主要成分FeTiO3 , 钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如图1: 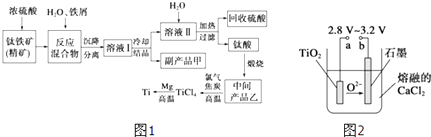
回答下列问题:
(1)钛铁矿和浓硫酸反应的产物之一是TiOSO4 , 反应中无气体生成.副产品甲阳离子是 .
(2)上述生产流程中加入铁屑的目的是 .
(3)此时溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子.常温下,其对应氢氧化物的Ksp如下表所示.
氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
Ksp | 8.0×10﹣16 | 1.0×10﹣29 | 1.8×10﹣11 |
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018molL﹣1 , 当溶液的pH等于时,Mg(OH)2开始沉淀.
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,写出该反应的离子方程式:
(4)Mg还原TiCl4过程中必须在1070K的温度下进行,你认为还应该控制的反应条件是 .
(5)在800~1000℃时电解TiO2也可制得海绵钛,装置如图2所示.图中b是电源的极,阴极的电极反应式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,一个装满氧气的容器质量为74g,若装满氮气时质量是66g,此容器的体积是( )
A. 4.48L B. 11.2L C. 22.4L D. 44.8L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质依次满足如图所示转化关系的是(图中箭头表示一步转化)( )
a | b | c | d | |
① | Si | SiO2 | H2SiO3 | Na2SiO3 |
② | N2 | NO | NO2 | HNO3 |
③ | Cu | CuO | Cu(OH)2 | CuSO4 |
④ | Na | NaOH | Na2CO3 | NaHCO3 |
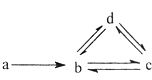
A.①②
B.②③
C.③④
D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com