
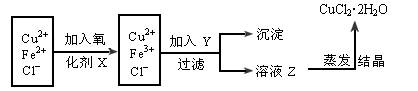
已知Cu2+、Fe2+在PH为4~5时不水解,而Fe3+却几乎完全水解而沉淀。请回答以下问题:
(1)X是什么物质________,其反应的离子方程式为_________________________。
(2)Y物质应具备的条件是________,生产中Y可选用________(写化学式)。
(3)溶液Z在蒸发结晶时应注意_________________。
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:022
工业上制取纯净CuCl2×2H2O的主要过程是:①将粗氧化铜(含少量铁)溶解于稀盐酸中,加热、过滤,调节滤液的pH为3;②对①所得滤液按下列步骤如图所示进行操作。
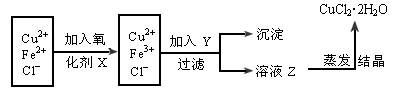
已知Cu2+、Fe2+在PH为4~5时不水解,而Fe3+却几乎完全水解而沉淀。请回答以下问题:
(1)X是什么物质________,其反应的离子方程式为_________________________。
(2)Y物质应具备的条件是________,生产中Y可选用________(写化学式)。
(3)溶液Z在蒸发结晶时应注意_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:

已知Cu2+、Fe2+在pH为4—5时不水解,而Fe3+却几乎完全水解而沉淀。请回答下列问题:
(1)X是什么物质?_________。其反应的离子方程式是_______________________________。
(2)Y物质应具备的条件是______________________,生产中Y可选:__________________。
(3)溶液乙在蒸发结晶时应注意:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
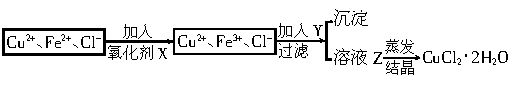
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com