
【题目】欲用98%的浓硫酸(ρ=1.84g·cm-1)配制为1mol·L-1的稀硫酸100ml。
(1)选用的主要仪器有:
①玻璃棒,②_________,③胶头滴管,④量筒,⑤__________。
(2)需要用量筒量取98%的浓硫酸________ml。
(3)请将下列各操作,按正确的序号填在横线上。
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至刻度线
D.洗净2~3次并转入容量瓶
E.稀释浓H2SO4
F.将溶液转入容量瓶
其操作正确的顺序依次为_____________________。
(4)简要回答下列问题:
①如果实验室有10mL、20mL、50mL的量筒,则所需的浓硫酸应选用____________mL的量筒最好
②任何实验都有误差,下列哪些操作会使所配的溶液浓度偏大____________
A.配置前,量取浓硫酸时发现量筒不干净用水洗净后直接量取
B.将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并用玻璃棒不断搅拌,若搅拌过程中有液体溅出
C.在转入容量瓶前烧杯中液体未冷却至室温
D.洗涤烧杯和玻璃棒2~3次,洗涤液未转入容量瓶
E.定容时俯视
【答案】(1)100mL容量瓶、烧杯 (2) 5.4 (3)AEFDCB (4)①10 ②CE
【解析】试题分析:(1)操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用量筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,由提供的仪器可知还需要仪器有:100mL容量瓶、烧杯;
(2)浓H2SO4的物质的量浓度c=![]() mol/L=18.4mol/L,根据稀释定律,稀释前后溶质硫酸的物质的量不变,设浓硫酸的体积为xmL,所以xmL×18.4mol/L=100mL×1mol/L,解得:x≈5.4mL;
mol/L=18.4mol/L,根据稀释定律,稀释前后溶质硫酸的物质的量不变,设浓硫酸的体积为xmL,所以xmL×18.4mol/L=100mL×1mol/L,解得:x≈5.4mL;
(3)操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,操作正确的顺序依次为AEFDCB;
(4)①量取5.4mL浓硫酸,需要使用10mL的量筒;②A.量取时发现量筒不干净用水洗净后直接量取,浓硫酸被蒸馏水稀释,导致浓硫酸的浓度偏低;B.在配制过程中将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并用玻璃棒不断搅拌,防止爆沸,迅速散热,若搅拌过程中有液体溅出,会导致溶质硫酸的物质的量偏低,配制的溶液浓度偏低;C.浓硫酸稀释放热,溶液的温度升高,转移前必须冷却稀释的溶液,否则导致配制的溶液温度较高,体积偏大,冷却后配制的溶液的体积偏低,最终导致浓度偏高;D.洗涤烧杯和玻璃棒2~3次,洗涤液也要转入容量瓶,否则会否则配制的溶液中,溶质物质的量减小,浓度偏低;E.定容时俯视,液面低于刻度线,溶液浓度偏高;故选CE。


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】“绿色化学”是当今社会提出的一个新概念。在该工艺中,理想状态是反应中原子全部转化为目标产物,即原子利用率为100%。利用以下各种化学反应类型的合成过程最符合绿色化学的是
A. 取代反应 B. 水解反应 C. 加聚反应 D. 酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于平衡常数的说法中,正确的是
A. 从平衡常数的大小可以推断一个反应进行的程度
B. 在任何条件下,化学平衡常数是一个恒定值
C. 平衡常数的大小只与浓度有关,而与温度、压强、催化剂等无关
D. 在平衡常数表达式中,反应物浓度用初始浓度,生成物浓度用平衡浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上食用油的生产大多数采用浸出工艺。菜籽油的生产过程为:将菜籽压成薄片,用轻汽油浸泡,进行操作A;过滤,得液体混合物;对该混合物进行操作B,制成半成品油,再经过脱胶、脱色、脱臭即制成食用油。操作A和B的名称分别是
A.溶解、蒸发 B.萃取、蒸馏 C.分液、蒸馏 D.萃取、过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为两个原电池装置图,由此判断下列说法错误的是( )

A.当两电池转移相同电子时,生成和消耗Ni的物质的量相同
B.两装置工作时,盐桥中的阴离子向负极移动,阳离子向正极移动
C.由此可判断能够发生2Cr3++3Ni=3Ni2++2Cr和Ni2++Sn=Sn2++Ni的反应
D.由此可判断Cr、Ni、Sn三种金属的还原性强弱顺序为:Cr>Ni>Sn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺流程如下:
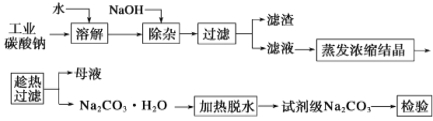
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:
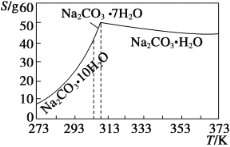
回答下列问题:
(1)滤渣的主要成分为_____________________________。
(2)“趁热过滤”的原因是_________________________。
(3)若在实验室进行“趁热过滤”,可采取的措施是________(写出一种)。
(4)已知:Na2CO3·10H2O (s)===Na2CO3(s)+10H2O(g) ΔH1= +532.36 kJ·mol-1
Na2CO3·10H2O(s)===Na2CO3·H2O(s)+9H2O(g) ΔH2= +473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
成分 | 质量(g) | 摩尔质量(g ·mol-1) |
蔗糖 | 50.00 | 342 |
硫酸钾 | 0.50 | 174 |
阿司匹林 | 0.35 | 180 |
高锰酸钾 | 0.50 | 158 |
硝酸银 | 0.04 | 170 |
⑴下列“鲜花保鲜剂”的成分中,属于非电解质的是 。
A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银
⑵“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为 mol.L-1。(只要求写表达式,不需要计算)
⑶配制上述1 L“鲜花保鲜剂”所需的仪器有:烧杯、玻璃棒、药匙、 、 、 。(在横线上填写所缺仪器的名称)
⑷在溶液配制过程中,下列操作正确且对配制结果没有影响的是 。
A.将药品放入容量瓶中加蒸馏水溶解
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能在溶液中大量共存的离子组是( )
A. H+、Na+、CO32—、Cl— B. Ba2+、Na+、Cl—、SO42—
C. K+、H+、SO42—、OH— D. Ag+、Al3+、NO3—、H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,有可逆反应:2A(g)+2B(g) ![]() C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
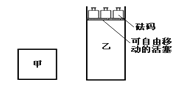
关于两容器中反应的说法正确的是( )
A.两容器达平衡后升高相同的温度时,甲容器的反应速率大于乙容器的速率
B.两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的密度不同
C.甲容器中的反应先达到化学平衡状态
D.在甲容器中再充入2mol A和2 mol B,平衡后甲中物质C的物质的量是乙中物质C的物质的量的2倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com