
����Ŀ����һ�������£���3 mol A��1 mol B�����������ڹ̶��ݻ�Ϊ2 L���ܱ������У�������Ӧ��![]() ��2 minĩ�÷�Ӧ�ﵽƽ�⣬�������0.8 mol D��0.4 mol C�������жϲ���ȷ����
��2 minĩ�÷�Ӧ�ﵽƽ�⣬�������0.8 mol D��0.4 mol C�������жϲ���ȷ����
A.![]() =1
=1
B.2 minʱ��A��Ũ��Ϊ0.9 mol��L-1
C.2 minʱ��A��ƽ����Ӧ����Ϊ0.3 mol��L-1��min-1
D.2 minʱ��B��ƽ����Ӧ����Ϊ0.9 mol��L-1��min-1
 �п������п��Ծ����ϵ�д�
�п������п��Ծ����ϵ�д� ��������״Ԫ��ϵ�д�
��������״Ԫ��ϵ�д� �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ͭþ�Ͻ���ȫ�ܽ���
ͭþ�Ͻ���ȫ�ܽ���![]() ���ܶ�Ϊ
���ܶ�Ϊ![]() ����������Ϊ
����������Ϊ![]() ��Ũ�����У��õ�
��Ũ�����У��õ�![]() ����
����![]() ��״��
��״��![]() ����Ӧ�����Һ�м���������
����Ӧ�����Һ�м���������![]() ��Һ��ǡʹ��Һ�еĽ�������ȫ������������˵������ȷ����
��Һ��ǡʹ��Һ�еĽ�������ȫ������������˵������ȷ����![]()
![]()
A.��Ũ������HNO3�����ʵ���Ũ����14 mol/L
B.����NaOH��Һ�������160 mL
C.�������Ե���������ʵ���Ϊ0.16 mol
D.�õ��Ľ�����������ij���Ϊ6.24 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ���һ��������������Ʒ�Ӧ�Ʊ���������(2NO+Na2O2=2NaNO2��2NO2+Na2O2=2NaNO3��NO�ܱ�����KMnO4��Һ����ΪNO3-)������˵���������

A.���װ�������Ժ�Ӧ�ȴ�ֹˮ�У��ӵ�����ͨ��N2
B.װ��C����������CO2��
C.D���п��ܺ��е�����ΪNaNO3��NaOH
D.װ��E���ڴ���β������Ӧ���������뻹ԭ�������ʵ���֮��Ϊ1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о���Ӧ���̵������仯����������������Ҫ���塣
��.�״�����Ҫ�Ļ���ԭ�ϡ����úϳ���(��Ҫ�ɷ�ΪCO��CO2��H2)��һ�������ºϳɼ״����밴Ҫ��ش��������⣺
(1)��ӦCO2(g)��3H2(g) ![]() CH3OH(g)��H2O(g)��ʹ�ú�δʹ�ô���ʱ����Ӧ���̺������Ķ�Ӧ��ϵ��ͼ��ʾ������˵����ȷ����___(����ĸ����)��
CH3OH(g)��H2O(g)��ʹ�ú�δʹ�ô���ʱ����Ӧ���̺������Ķ�Ӧ��ϵ��ͼ��ʾ������˵����ȷ����___(����ĸ����)��

A���ÿ��淴Ӧ������ӦΪ���ȷ�Ӧ
B�����ѷ�Ӧ���еĻ�ѧ�������յ�������С���γ��������еĻ�ѧ�����ͷŵ�������
C������b��ʹ���˴�����Ӧ�����ߣ��Ҽ��������Ӧ�ȱ�С
(2)CO��CO2��H2�ںϳɹ����з�������Ҫ��Ӧ���£�
��CO(g)��2H2(g) ![]() CH3OH(g)����H1����99 kJ��mol��1
CH3OH(g)����H1����99 kJ��mol��1
��CO2(g)��3H2(g) ![]() CH3OH(g)��H2O(g)����H2����58 kJ��mol��1
CH3OH(g)��H2O(g)����H2����58 kJ��mol��1
��CO2(g)��H2(g) ![]() CO(g)��H2O(g)����H3
CO(g)��H2O(g)����H3
����H3��____��
(3)ֱ�Ӽ״�ȼ�ϵ��(���DMFC)������ṹ������ת���ʸߡ��Ի�������Ⱦ������Ϊ������Դ�����Ʒ��Խ��Խ�ܵ���ע��DMFC�Ĺ���ԭ����ͼ��ʾ��

��ͨ��a����ĵ缫�ǵ�ص�____(����������������)������缫��ӦʽΪ___��
��.��֪��������ͨ����������S8(б����)����ʽ���ڣ���������״̬�£���S2��S4��S6��S8�ȶ���ͬ�������壬����S4��S6��S8�������ƵĽṹ�ص㣬��ṹ��ͼ��ʾ��
![]()
(1)��һ���¶��£������������ƽ��Ħ������Ϊ80 g��mol��1�����������S2�����������С��_____��
(2)����֪�������ļ���Ϊd kJ��mol��1���������ļ���Ϊe kJ��mol��1��S(s)��O2(g)===SO2(g)��H����a kJ��mol��1����S8��������ļ���Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ײʱ����ȫ�����з�����Ӧ![]() ������2 mol N2���ɣ��������ж���ȷ����( )
������2 mol N2���ɣ��������ж���ȷ����( )
A.N2�����Ϊ44. 8 L
B.�� 0. 125 mol KNO3������
C.N2���������������ǻ�ԭ����
D.ת�Ƶ��ӵ����ʵ���Ϊ10 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ������װ���Ʊ�������Cl2�����ʡ�����˵����ȷ����
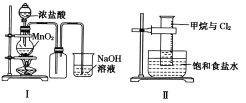
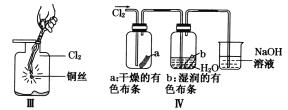
A. Iͼ�У����MnO2������Ũ����Ϳ�ȫ��������
B. IIͼ�У���Ͳ�з����˼ӳɷ�Ӧ
C. IIIͼ�У�������ɫ����
D. IVͼ�У�ʪ�����ɫ��������ɫ��������Һ�����ձ��У�����Һ�����ԣ������Cl2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��10��1�����л���������70���꣬�����ڼ�Դ��������ʻ�ʩ����S-�տ����Ƽ��Ա�֤�ʻ�ʢ����S-�տ��صķ��ӽṹ��ʽ��ͼ�����й��ڸ����ʵ�˵����ȷ����
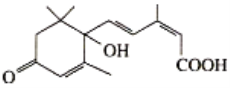
A.���л���ķ���ʽΪC15H20O4
B.���л����ܷ���ȡ�����ӳɺ�ˮ�ⷴӦ
C.1mol�ĸ��л������������Ʒ�Ӧ����2molH2
D.1mol���л��ﺬ��4mol˫��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС��Ϊ���о���������Ի�ѧ��Ӧ���ʵ�Ӱ�죬���������Ը�����������ķ�Ӧ����¼����ʵ�����ݣ���֪![]() Ϊ����٤��������ֵ����
Ϊ����٤��������ֵ����
�Թ��������Լ���������/mL | ��Һ������ɫ����ʱ��/min | |||||
ʵ���� | ʵ���¶�/�� | 0.6 mol/LH2C2O4��Һ | H2O | 3 mol/LH2SO4��Һ | 0.05 mol/LKMnO4��Һ | |
�� | 25 | 3.0 | v1 | 2.0 | 3.0 | 1.5 |
�� | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
�� | 50 | 2.0 | v2 | 2.0 | 3.0 | 1.0 |
��1����д���÷�Ӧ�����ӷ���ʽ��___�����÷�Ӧ��ʵ��������ݷ�Ӧ��ȫʱת�Ƶ�����Ϊ_____![]() ��
��
��2��ʵ��٢���̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬ʵ��ڢ�ʱ̽���¶ȶԷ�Ӧ���ʵ�Ӱ�죬�����V1=_______��V2=__________��
��3������ʵ��١��ڵ����ݣ����Եõ��Ľ�����____��
��4����С��ͬѧ���ݾ��������n��Mn2+����ʱ��仯��������ͼ1��ʾ������ͬѧ�������е�ʵ�����Ϸ��֣���ʵ�������n��Mn2+����ʱ��仯��ʵ��������ͼ2��ʾ��

��С��ͬѧ����������Ϣ������µļ��裬�����һ��ʵ�鷽����������ʵ��̽����
ʵ���� | ʵ���¶�/�� | �Թ��������Լ���������/ml | �ټ���ij�ֹ��� | ��Һ������ɫ����ʱ��/min | |||
0.6 mol/LH2C2O4��Һ | H2O | 3 mol/LH2SO4��Һ | 0.05 mol/L KMnO4 ��Һ | ||||
�� | 25 | 3.0 | 2.0 | 2.0 | 3.0 | MnSO4 | t |
�ٸ�С��ͬѧ������¼�����__________��
������С��ͬѧ����ļ��������Ӧ�۲쵽__________����ʵ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС����������������Ʒ������ȼ��仯�������̽����
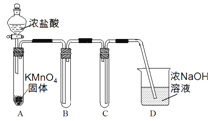
��.�ø�����غ�Ũ���ᷴӦ��ȡ����
��1����С��������ͼװ�ü��Լ��Ʊ����ռ�����Cl2��װ��B��C�����÷ֱ���___________��_______________��
��2���Ƶõ������м�������ˮ���õ�������ˮ��������ˮ�к���Ԫ�ص�����____________��д��ȫ��������
��3��������ˮ��ʯ��ʯ�ķ�Ӧ����ȡ��ŨHC1O��Һ�ķ���֮һ���ڹ�����ʯ��ʯ�м��뱥����ˮ��ַ�Ӧ�����������ݲ�������Һdz����ɫ��ȥ�����ˣ��õ�����Һ��Ư���Աȱ�����ˮ��ǿ��
����ҺƯ������ǿ��ԭ����________________���û�ѧƽ���ƶ�ԭ�����ͣ���
��������ˮ��ʯ��ʯ��Ӧ����HC1O�ķ���ʽ��___________________��
��. ClO3����Cl����H+��Ӧ��̽��
��4��KClO3��KCl��������Է�Ӧ����С�������ϵ��ʵ���о���Ӧ�����Է�Ӧ��Ӱ�죬ʵ���¼���£�ʵ���������½��У���
�ձ���� | 1 | 2 | 3 | 4 |
����ر�����Һ | 1mL | 1mL | 1mL | 1mL |
�Ȼ��ع��� | 1g | 1g | 1g | 1g |
ˮ | 8mL | 6mL | 3mL | 0mL |
���ᣨ6mol/L�� | 0mL | 2mL | (____)mL | 8mL |
���� | ������ | ��Һ��dz��ɫ | ��Һ�ʻ���ɫ������dz����ɫ���� | ��Һ�ʻ���ɫ�� |
����ϵ��ʵ���Ŀ��_______________________��
���ձ�3ȡ����������ӦΪ______________mL��
��5����С��ͬѧ�����ϵ�֪��������ع����Ũ������Ҳ������������ͬʱ�д���ClO2���ɣ�ClO2�е�Ϊ10�����۵�Ϊ��59����Һ��Ϊ��ɫ��Cl2�е�Ϊ��34����Һ̬Ϊ����ɫ��������ʵ����֤Cl2�к���ClO2______________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com