
����Ŀ������ӵ���봫ͳ�����ȣ������죬�����ܶȸ��ߣ�ʹ��ʱ����������ֻ��ͱʼDZ����Եȱ�Яʽ���Ӳ�Ʒ�Ϲ㷺Ӧ�á���ҵ�ϳ���﮻Կ�(��Ҫ�ɷ�Ϊ LiAlSi2O6��������FeO��MgO��CaO������)Ϊԭ������ȡ����ﮣ�����һ�ֹ�����������

��֪
�ٲ��ֽ����������↑ʼ��������ȫ����ʱ��pH��

��Li2CO3���ܽ�����¶ȱ仯��ͼ��ʾ��
�Իش��������⣺
(1)���ʱ��Ϊ����߽�ȡ�ʿɲ�ȡ�����¶ȡ������ʯ�����衢���˺��ٴν�ȡ�ȴ�ʩ����ͨ��_______����߽�ȡ�ʡ�
(2)��ӦI��Ӧ����pH��ΧΪ_______������A�ijɷֳ�H2SiO3��CaCO3��Al(OH)3�⣬����___________��
(3)��Ӧ������ӷ���ʽΪ_________________��
(4)������I��������Ϊ______��ϴ��Li2CO3����Ҫʹ��___(ѡ������ˮ��������ˮ��)��������_________��
(5)��֪�(Rb)��������ܵIJ��ϣ������ͬ���塣�� amol CH3 COORb����ˮ�����Һ�������Һ�еμ� bLc mol��L�������Һ�����ԡ���c=_______(�ú�a��b��ʽ�ӱ�ʾ����֪25��ʱ��CH3COOH����ƽ�ⳣ��ka��2![]() 10��5)��
10��5)��
���𰸡��ӳ���ȡʱ�䣨���������Ũ�ȣ� 4.7~9.6 Fe(OH)3��CaSO4 Mg2����2OH����Mg(OH)2�� (��Mg2����Ca(OH)2��Ca2+��Mg(OH)2��) Ca2+��CO32-= CaCO3�� ���� ��ˮ ̼��﮵��ܽ�����¶����߶����ͣ���ˮϴ�ӿ��Լ���̼��﮵��ܽ���ʧ ![]()
��������
��1����߽�ȡ�ʣ����������Ũ�ȡ������¶ȡ��������������������ӳ���ȡʱ��ȣ�
(2)��ӦI�е���pH��Ŀ���dz�ȥMg2+��Al3+��
(3)��Ӧ�����pH=11��Ŀ���dz�ȥMg2����
(4)������I��Ŀ���Ƿ��������̼��ﮣ�����̼��﮵��ܽ�����¶����߶����ͷ�����
(5)����![]() ��������Ũ�ȡ�
��������Ũ�ȡ�
��1���������Ũ�ȡ������¶ȡ��������������������ӳ���ȡʱ�������߽�ȡ�ʣ�����Ϊ����߽�ȡ�ʿɲ�ȡ�����¶ȡ������ʯ�����衢���˺��ٴν�ȡ�ȴ�ʩ����ͨ���ӳ���ȡʱ����������Ũ������߽�ȡ�ʣ�
(2)��ӦI�е���pH��Ŀ���dz�ȥFe3+��Al3+�����Ե���pH��ΧΪ4.7��9.6�����������ˮ�����Գ���A�ijɷֳ�H2SiO3��CaCO3��Al(OH)3�⣬����Fe(OH)3��CaSO4��
(3)��Ӧ�����pH=11��Ŀ���dz�ȥMg2������Ӧ����Ҫ���ӷ���ʽ��Mg2����2OH����Mg(OH)2����
(4)������I��Ŀ���Ƿ��������̼��ﮣ����ԡ�����I���ǹ��ˣ�̼��﮵��ܽ�����¶����߶����ͣ���ˮϴ�ӿ��Լ���̼��﮵��ܽ���ʧ������ϴ��Li2CO3����Ҫʹ����ˮ��
(5) �� amol CH3 COORb����ˮ�����Һ�������Һ�еμ� bLc mol��L�������Һ�����ԡ����Ϻ���Һ�����ΪV�����������غ㣬c(CH3COOH)��c(CH3COO��)��(a+bc)/V�����ݵ���غ㣬c(CH3COO��) �� c(Rb+)��a/V������c(CH3COOH)��bc/V��![]() ��
��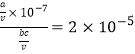 ������c=
������c=![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������NaBH4��ZnCl2�������¿�ת��Ϊ��������NaBH4ת��ΪH3BO3��

(1)Zn2+��̬��������Ų�ʽΪ_____��
(2)���״�(![]() )��̼ԭ�ӵ��ӻ��������Ϊ_____��
)��̼ԭ�ӵ��ӻ��������Ϊ_____��
(3)1mol���������(![]() )�����к�����������ĿΪ_____mol��
)�����к�����������ĿΪ_____mol��
(4)��BH4����Ϊ�ȵ������������Ϊ_____(�ѧʽ)��BH4�����ӵĿռ乹��Ϊ(����������)_____��
(5)������һ�ֲ�״�ṹ��ɫ���壬���ڵ�H3BO3����ͨ���������(��ͼ��ʾ)��1molH3BO3��������_____mol�����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʯ�е�һ�֣�����Ҫ�ɷ�Ϊ��������NaAl(Si2O6)��������Cr��Ni��Mn��Mg��Fe��Ԫ�ء��ش��������⣺
(1)Cr3+�����Ų�ʽΪ______________________����̬Siԭ���У�����ռ�ݵ�����ܲ����Ϊ______________________��
(2)�������Ҫ�ɷ�Ϊ�������ƣ�����Ԫ�صĵ�һ�������ɴ�С��˳��___________��
(3)�̵�һ�ֻ�����Ļ�ѧʽΪMn(BH4)2(THF)3��THT�Ľṹ��ʽ��ͼ��ʾ��

��THF��Cԭ�ӵ��ӻ��������Ϊ___________����BH4���Ŀռ乹��Ϊ___________
��NaBH4������ѧ��������_____________
A�����Ӽ� B�����ۼ� C����� D����λ��
(4)MnO���۵�(1660��)��MnS���۵�(1610��)�ߣ�ԭ��______________________��
(5)Ni�����γɶ������������һ��NixO����ľ����ṹΪNaCl�ͣ����ھ���ȱ�ݣ�xΪ0.88���Ҿ�����Ni�Ĵ�����ʽΪNi2+��Ni3+��������N i2+��Ni3+���������Ϊ___________���þ���ľ�������Ϊ428pm�������ܶ�Ϊ___________g��cm��3(NA��ʾ�����ӵ�������ֵ���г�����ʽ����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������������һ����̼�������з�Ӧ��Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
��1���÷�Ӧ��ƽ�ⳣ������ʽΪK=________��
��2�����¶��£���2 Lʢ��Fe2O3��ĩ���ܱ�������ͨ��CO���壬10 min�������˵�����11.2 g����10 min��CO��ƽ����Ӧ����Ϊ________��
��3���÷�Ӧ�ﵽƽ�����Fe�ۣ�ƽ��________�ƶ������ֺ��º���ͨ��CO��ƽ����________�ƶ���������������ҡ�������
��4�������÷�Ӧ�Ѵ�ƽ��״̬����______________
A.��λʱ��������nmolCOͬʱ����nmolCO2 B.����ʱ��������ѹǿ����
C.������������������ D.CO2������������� E.Fe��Ũ�Ȳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2.0 molPCl3��1.0 molCl2�������������ܱ������У���һ�������·���������Ӧ��
PCl3(g)+ Cl2(g)![]() PCl5(g)�ﵽƽ��ʱ�� PCl5Ϊ0.40 mol�������ʱ����1.0 molPCl3��0.50 molCl2������ͬ�¶����ٴ�ƽ��ʱ PCl5�����ʵ�����
PCl5(g)�ﵽƽ��ʱ�� PCl5Ϊ0.40 mol�������ʱ����1.0 molPCl3��0.50 molCl2������ͬ�¶����ٴ�ƽ��ʱ PCl5�����ʵ�����
A. 0.40 mol B. ��0.20 mol C. 0.20 mol D. ����0.20 mol����0.40 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���黯��(GaAs)�������İ뵼����ϣ������������ͼ�������̫���ܵ�صIJ��ϵȡ�

�Իش���������
(1)д����̬Asԭ�ӵĺ�������Ų�ʽ_______��
(2)����Ԫ�������ɣ�ԭ�Ӱ뾶Ga _____As(������������<����ͬ)����һ������Ga _____As
(3)AsCl5���ӵ����幹��Ϊ___________������As���ӻ��������Ϊ_______��
(4)GaF3���۵����1000�棬GaCl3���۵�Ϊ79�棬��ԭ����________��
(5)GaAs���۵�Ϊ1238�棬�侧���ṹ��ͼ��ʾ���þ��������Ϊ_______����As��_____�����ϡ���֪�����ӵ�����ΪNA����������![]() ��lnm���˾�����ܶ�Ϊ_____ g��cm��3(д������ʽ)��
��lnm���˾�����ܶ�Ϊ_____ g��cm��3(д������ʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ˮ�п��ܴ��ڵ���ƽ�⡢�ε�ˮ��ƽ��ͳ������ܽ�ƽ�⣬���Ƕ��ɿ�����ѧƽ�⡣�������ѧ֪ʶ�Ļش�
��1��AΪ0.1 mol��L��1��(NH4)2SO4��Һ���ڸ���Һ�и������ӵ�Ũ���ɴ�С˳��Ϊ____________________________��
��2��BΪ0.1 mol��L��1NaHCO3��Һ����NaHCO3��Һ�д��ڵĸ���ƽ����ϵΪ�������ӷ���ʽ��ʾ����________________________________________________________________________________________________________________________________________________��ʵ����NaHCO3��Һ��pH > 7�������NaHCO3��Һ�Լ��Ե�ԭ��_________________________��
��3��CΪFeCl3��Һ��ʵ����������FeCl3��Һʱͨ����Ҫ�����м�������Ŀ����________________________________________������B��C��Һ��ϣ����������ɫ��������ɫ���壬�÷�Ӧ�����ӷ���Ϊ___________________________________��
��4��DΪ��������AgCl����ı�����Һ���Ȼ�����ˮ�д��ڳ����ܽ�ƽ�⣺AgCl(S) ![]() Ag+(aq)+ Cl��(aq)����25��ʱ���Ȼ�����Ksp = 1.8��10��10mol2��L��2���ֽ������Ȼ����ֱ���룺��100mL����ˮ�У���100mL 0.2 mol��L��1AgNO3��Һ�У���100mL 0.1 mol��L��1�Ȼ�����Һ�У���100mL 0.1 mol��L��1������Һ�С���ֽ�������ͬ�¶���������Ũ���ɴ�С��˳����____________����д��ţ�
Ag+(aq)+ Cl��(aq)����25��ʱ���Ȼ�����Ksp = 1.8��10��10mol2��L��2���ֽ������Ȼ����ֱ���룺��100mL����ˮ�У���100mL 0.2 mol��L��1AgNO3��Һ�У���100mL 0.1 mol��L��1�Ȼ�����Һ�У���100mL 0.1 mol��L��1������Һ�С���ֽ�������ͬ�¶���������Ũ���ɴ�С��˳����____________����д��ţ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������﮵��Ӧ�ù㷺�� ��طŵ��������Ҫ����Li4Ti5O12�� ����������Fe�� ��ͨ�����й������̻����ѡ� ﮡ��ش��������⣺

(1) Li4Ti5O12�У� TiԪ�صĻ��ϼ�Ϊ___�� ��Һ1�к���������������___(�����ӷ���)��
(2) ���ʱ Li4Ti5O12�����ķ�Ӧ�ǣ� Li4Ti5O12+7H2SO4+5H2O2��2Li2SO4+5[TiO(H2O2)]SO4+7H2O�� �÷�Ӧ�Ƿ�����������ԭ��Ӧ��___(�� ������ �� ������)�� ����1��___��
(3) ��[TiO(H2O2)]SO4��Һ�м���Na2SO3��Һ������Ӧ�����ӷ���ʽΪ___��
(4) ��TiOSO4��Һ��ͨ��NH3������Ӧ�����ӷ���ʽΪ___��
(5) ����TiO(OH)2������ˮϴ�ӵ�Ŀ����___��
(6) ��ȡʱ�� �¶ȶ���ȡ�ʵ�Ӱ����ͼ��ʾ����ͼ����֪ʵ��ʱѡ���ڳ����½��м��ɣ� ������__��

(7)����ȡ�� �� ������ȡ�� �ɼ�ʾΪ��[TiO(H2O2)]2+��2(HA)2![]() [TiO(H2O2)](HA2)2��2H+������ȡ�����м�����Լ�X��___��
[TiO(H2O2)](HA2)2��2H+������ȡ�����м�����Լ�X��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�������������մɷ�ӦΪ3SiCl4��2N2��6H2![]() Si3N4��12HCl���йظ÷�Ӧ˵����ȷ����
Si3N4��12HCl���йظ÷�Ӧ˵����ȷ����
A. SiCl4�������� B. N2������ԭ��Ӧ
C. H2����ԭ D. N2ʧ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com