
【题目】溶液、胶体和浊液这三种分散系的本质区别是( )
A. 是否有丁达尔现象 B. 是否能通过滤纸
C. 分散质粒子的大小 D. 是否均一、透明、稳定
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】如图可逆反应A+2B![]() 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
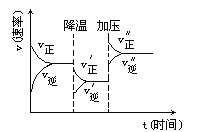
A.正反应是吸热反应 B.若A、B是气体,则D是液体或固体
C.改变物质浓度,平衡不会移动 D.A、B、C、D均为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol/L NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A.60 mL B.45 mL C.30 mL D.15 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学一选修3:物质结构与性质】X、Y、Z、W四种元素的部分信息如下表所示。
元素 | X | Y | Z | W |
相关 信息 | 短周期元素,最高化合价为 +7价 | 基态原子中,电子占据的最高能层符号为L,最高 能级上只有两个自旋方向相同的电子 | 核外电子共有15种运动状态 | 能与X形成两种常见化合物WX2、WX3,酚遇WX3溶液能发生显色反应 |
回答下列问题:
(1) W的基态原子电子排布式为____, X、Y、Z三种元素电负性由大到小的顺序为___(用具体的元素符号填写)。
(2)化合物YX4、ZX3、ZX5 (气态或液态时)中,中心原子的轨道类型不是sp3杂化的是________(填化学式,下同),分子构型是正四面体的是______, 属于极性分子的是____。
(3)已知WX3的熔点:306℃,沸点:319℃,则WX3的晶体类型为____,Y与氢元素能形成YnH2n+2 (n为正整数)的一系列物质,这一系列物质沸点的变化规律以及影响的因素是______________。
(4)Z可形成多种含氧酸,如H3ZO4、HZO3、H3ZO3等,其中酸性最强的是______(填化学式)。
(5)W元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如下图所示。在面心立方晶胞中W原子的配位数为___;若W的原子半径为r cm,阿伏加德罗常数为NA,则其体心立方晶体的密度可表示为_____gcm-3。
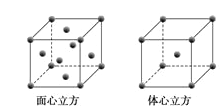
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂拟综合处理含NH4-废水和工业废气(主要含N2、CO2、.SO2、NO、CO,不考虑其它成分),设计了如下流程:
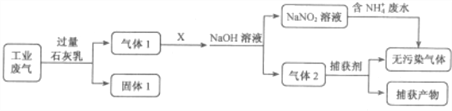
已知:NO+NO2+2NaOH=2NaNO2+H2O
回答下列问题:
(1)固体1的主要成分Ca(OH)2、CaCO3和______。
(2)气体X与气体1反应时起到的作用是______(填“氧化剂”、“还原剂”或“即不是氧化剂也不是还原剂”),捕获剂所捕获的气体主要是______ (填化学式)。
(3) NaOH溶液吸收等物质的量的NO、NO2气体过程中,当生成1molNaNO2时转移电子数为_______NA。
(4)用NaNO2溶液处理含NH4-废水时,发生反应的离子方程式为__________;含NH4-废水也可用沉淀法处理:Mg2++NH4- +PO43-=== MgNH4PO4↓, 已知25℃时,Ksp(MgNH4PO4)=2.5×10-13 。向废水中按比例投入镁盐和磷酸盐,欲使沉淀后废水中残留的铵态氮达到一级排放标准(≤1.0mg·L-1,即≤7.14×10-5 mol·L-1),且c(PO43-)=1.0×10-5 mol·L-1,则应使沉淀后的废水中c( Mg2+) ≥________。
(5)电化学氧化法是处理氨氮废水的一种新工艺。间接电氧化的原理是:向废水中加入一定量的氯离子,使其电解时在阳极放电生成氯单质,利用氯单质与水反应生成的次氯酸将NH4+氧化 为氮气。最后一步反应的离子方程式为__________________________。
(6) 已知25℃时,HNO2的电离常数Ks =5.1×10-4。实验室常用NaOH溶液吸收NO2尾气,反应为2NO2+ 2NaOH==NaNO3+ NaNO2+H2O。若用1L 0.4 mol·L-1Na(OH)溶液充分吸收0.4mol NO2气体,则所得溶液显___(填“酸性”、“碱性”或“中性”),原因是___________(用离子方程式表示);忽略溶液体积变化,近似计算所得溶液的pH≈____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
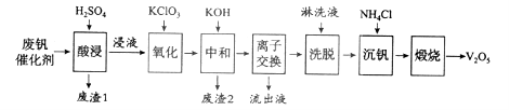
回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________,同时V2O4转成VO2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为______mol。
(3)“中和”作用之一是使钒以V4O124形式存在于溶液中。“废渣2”中含有_______。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V4O124![]() R4V4O12+4OH(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”、“碱”或“中”)。
R4V4O12+4OH(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”、“碱”或“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化合物的叙述,正确的是
A. 磷脂含有磷元素,脱氧核糖核酸不含氧元素
B. 维生素D属于脂质,能促进肠道对钾和磷的吸收
C. 能与双缩脲试剂产生紫色反应的只有蛋白质
D. 含有DNA和RNA的细胞生物中,DNA是遗传物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com