
����һ������ˮ��Һ��ֻ���ܺ������������е������֣�K+��NH4+��Cl����Ba2+��CO32����SO42������ȡ����100mL��Һ��������ʵ�飺
��һ�ݼ���AgNO3��Һ�г���������
�ڶ��ݼ�����NaOH��Һ���Ⱥ��ռ���0.04mol���壻
�����ݼ�����BaCl2��Һ�õ��������6.27g������������ϴ�ӡ������������Ϊ2.33g
�ۺ�����ʵ�飬����Ϊ���½�����ȷ���� (����)
A���û��Һ��һ�����У�K+��NH4+��CO32����SO42�������ܺ�Cl��
B���û��Һ�С������У�NH4+��CO32����SO42�������ܺ�K+��Cl��
C���û��Һ��һ�����У�NH4+��CO32����SO42����Cl�������ܺ�K+
D���û��Һ�У�c(K+) �� 0.02mol/L c(CO32��) = 0.02mol/L

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����������Ӧͼʽ��ȷ���� �� ��
| �� | �� | �� | �� | �� | �� | �� | �� | |
| ԭ�Ӱ뾶 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| ��Ҫ���ϼ� | -2 | +2 | +1 | +5��-3 | +7��-1 | +1 | +5��-3 | +3 |

A�������ж�����Ԫ�����ʵ������ƶ�Ԫ�آ�����������Ӧ��ˮ���������ǿ
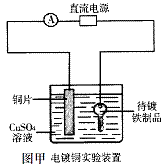
B��ͼ��װ���У���������ƷӦ���Դ��������
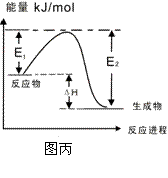
C��ͼ�ұ�ʾH2��O2������Ӧ�����е������仯����H2��ȼ���ȵ��Ȼ�ѧ����ʽΪ��
2H2(g)+O2(g)=2H2O(g) ��H= �� 483.6 kJ/mol
D��ͼ����ʾijһ���ȷ�Ӧ����ʹ�ô���E1��E2����H���ᷢ���ı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��״�л�������к���m�� ��CH3 ��n�� ��CH2�� ��a�� ������Ϊ ��NH2����NH2����Ŀ������
������Ϊ ��NH2����NH2����Ŀ������
A��2n + 3��m B��a + 2��m C��n + m + a D��a + 2n + 2��m
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���м���˵������ȷ���� (����)
A��Ħ���ǻ�ѧ�ϳ��õ�һ��������
B��ij���ʺ���6.02��1023���������������Ŀ��������һ����1 mol
C��1Ħ���������ӿ��Ա�ʾΪ1 mol H2
D�������Ħ������Ϊ98 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ҺCl�����ʵ���Ũ����50 mL 1 mol��L��1AlCl3��Һ��Cl�����ʵ���Ũ����ȵ���( )
A��150 mL 1 mol��L��1NaCl��Һ B��75 mL 1.5 mol��L��1CaCl2��Һ
C��150 mL 3 mol��L��1KClO3��Һ D��50 mL 3 mol��L��1MgCl2��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijͬѧ����ˮ�ʼ��վ����900mL 1 mol��L��1NaOH��Һ��
��1����ͬѧӦѡ��_________mL������ƿ��
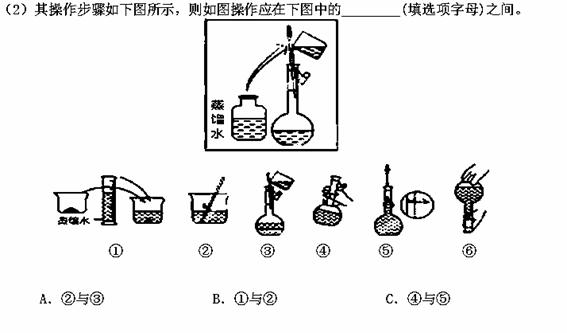
��3����ͬѧӦ��������ƽ��ȡNaOH���� g��������Ϊ33.1 g���ձ�����������ƽ�ϳ�ȡ����NaOH����ʱ��������ͼ��ѡ������ȷ��ʾ����λ�õ�ѡ�� ����ѡ����ĸ����
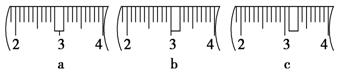
��4�����в�����������Һ��Ũ�ȴ�С�к�Ӱ�� (�ƫ����ƫС������Ӱ�족)��
�ٶ���ʱ�����Ӷ�����Ũ�Ȼ� ��
��ת����Һ�����У�����Һ�彦������Ũ�Ȼ� ��
������ƿδ���Ũ�Ȼ� ��
�ܶ���ҡ�Ⱥ�����Һ������ڿ̶��ߣ�Ũ�Ȼ� ��
��5��������Һ��ʵ�ʲ��������У�����Ҫ�죬�������� ����ʹ���Ƶ�NaOH��Һ��Ũ�ȱ�1 mol��L��1 �����С������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����йط������Ϸ��е�����������ȷ���� �� ��
A.�Ϸ������Ϸ�������ɻ�������ɫ��Ⱦ������ȾԴ֮һ
B.���������ᡢ�������ܺ�
C.��������¯����ʳƷ
D.������ʢ�ź��ͽ϶��ʳƷ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������������������þ�Ļ����Һ1000mL�У�c(Al3+) = 0.2mol/L������������1.6mol/L KOH��Һʱ�����ɵij�����࣬�ټ��������KOH��Һ�����ˡ�ϴ�ӡ�����ð�ɫ����11.6g����Ӧǰ�Ļ����Һ��c(H2SO4)�� �� ��
A�� 0.20mol/L B��0.30mol/L C��0.40mol/L D��0.60mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�о�NO2��SO2���ȴ�����Ⱦ����Ĵ���������Ҫ���壮
��1��NO2����ˮ���գ���Ӧ�Ļ�ѧ��Ӧ����ʽΪ��3NO2+H2O=NO+2HNO3�������÷�Ӧ6NO2+8NH3 7N2+12H2OҲ�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״�����ǡ�6.72��L��
7N2+12H2OҲ�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״�����ǡ�6.72��L��
��2����֪��2SO2��g��+O2��g��⇌2SO3��g����H=��196.6kJ•mol��1
2NO��g��+O2��g��⇌2NO2��g����H=��113.0kJ•mol��1
��ӦNO2��g��+SO2��g��⇌SO3��g��+NO��g���ġ�H=����41.8��kJ•mol��1��
һ�������£���NO2��SO2�������1��2�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���ǡ�b����
a����ϵѹǿ���ֲ��� b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ��� d��ÿ����1mol SO3��ͬʱ����1molNO2
���������Ӧƽ��ʱNO2��SO2�����Ϊ1��6����ƽ�ⳣ��K=������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com