
【题目】某兴趣小组用Fe2(SO4)3溶液吸收含SO2的尾气(SO2的体积分数约10%,其余为空气),实验装置如图所示:
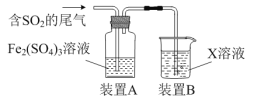
(1)装置A中SO2与Fe2(SO4)3溶液中反应生成FeSO4,写出该反应的化学方程式:___。
(2)反应后,若要检验装置A中Fe3+是否过量,可用试剂为___;若要检验SO2是否过量,可用试剂为___。
(3)装置B中所用X溶液为___,作用是___。
(4)若实验测得反应后的装置A中不含有SO2,为测定其中所含FeSO4的物质的量浓度,现进行如下实验:取20.00mL装置A中溶液,向其中逐滴加入0.1000mol·L-1Ce(SO4)2溶液,发生反应Fe2++Ce4+=Ce3++Fe3+,当反应恰好完全时,共消耗Ce(SO4)2溶液18.00mL。请通过计算确定FeSO4的物质的量浓度___(写出计算过程)。
【答案】SO2+Fe2(SO4)3+2H2O=2FeSO4+2H2SO4 KSCN溶液 品红溶液 NaOH溶液 吸收未完全反应的SO2,防止污染空气 ![]() ,
,![]()
【解析】
Fe3+具有一定的氧化性,SO2具有一定的还原性,因此用Fe2(SO4)3吸收SO2时二者会发生氧化还原反应;检验A中的Fe3+是否过量,即检验Fe3+是否剩余即可;若SO2过量,则选择试剂检验有SO2剩余即可;为了保证SO2吸收完全,防止其污染空气,需要用NaOH溶液对尾气再进行吸收;在计算确定FeSO4的浓度时,可利用题干中提供的方程式计算即可。
(1)装置A中SO2与Fe2(SO4)3发生的氧化还原反应的方程式为:SO2+Fe2(SO4)3+2H2O=2FeSO4+2H2SO4;
(2)检验Fe3+可用KSCN溶液,出现血红色物质,则证明Fe3+过量;检验SO2可用品红溶液,品红褪色,则证明SO2过量;
(3)通过分析可知,B装置中盛放的为NaOH溶液,作用是吸收未反应完的SO2,避免其造成空气污染;
(4)因为Ce4+与Fe2+反应时按照1:1反应,因此消耗的Ce(SO4)2的量即为FeSO4的量,即:![]() ,那么FeSO4的浓度为:
,那么FeSO4的浓度为:![]() 。
。


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案科目:高中化学 来源: 题型:
【题目】某课题组以甲苯为主要原料,采用以下路线合成镇静催眠药物——苯巴比妥:
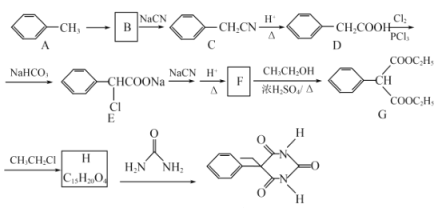
已知:![]() 。回答下列问题:
。回答下列问题:
(1)写出H的结构简式______________________。H→苯巴比妥的反应类型_________________。
(2)写出F→G的化学方程式________________________________。
(3)下列说法正确的是__________。
a.B的核磁共振氢谱有5组峰
b.化合物E能发生取代,氧化、加成、消去等反应
c.尿素在一定条件下可水解生成![]() 和
和![]()
d.苯巴比妥的分子式为![]()
(4)F制备G时会生成副产物![]() ,写出符合下列条件的M的同分异构体的结构简式: ___________________。
,写出符合下列条件的M的同分异构体的结构简式: ___________________。
①除苯环外不含其它环状结构。且苯环上有3个取代基;
②核磁共振氢谱图显示有5种化学环境不同的氢原子;
③该物质可发生银镜反应与水解反应,且1mol该物质完全水解时需要2molNaOH。
(5)以乙醇为原料可合成![]() ,请设计合成路线(用流程图表示,无机试剂任选)。___________
,请设计合成路线(用流程图表示,无机试剂任选)。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+4![]() +2H2O
+2H2O
B.氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
C.实验室用氯化铵和熟石灰制氨:![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
D.Cu与足量的浓硝酸:Cu+2![]() +4H+=Cu2++2NO2↑+2H2O
+4H+=Cu2++2NO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锶有“金属味精”之称。以天青石(主要含有SrSO4和少量CaCO3、MgO杂质)生产氢氧化锶的工艺如下:

已知氢氧化锶在水中的溶解度:
温度(℃) | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
溶解度(g/100mL) | 0.91 | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(1)隔绝空气焙烧时SrSO4只被还原成SrS,化学方程式为____。
(2)“除杂”方法:将溶液升温至95℃,加NaOH溶液调节pH为12。
①95℃时水的离子积KW=1.0×10-12,Ksp[Mg(OH)2]=1.2×10-10,则溶液中c(Mg2+)=____。
②若pH过大,将导致氢氧化锶的产率降低,请解释原因____。
(3)“趁热过滤”的目的是____,“滤渣”的主要成分为___。
(4)从趁热过滤后的滤液中得到Sr(OH)2产品的步骤为____、过滤、洗涤、干燥。
(5)“脱硫”方法:用FeCl3溶液吸收酸浸产生的气体,吸收时的氧化产物为___(填化学式);再用石墨电极电解吸收液,电解后可在“脱硫”中循环利用的物质是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇和乙酸是生活中常见的有机物。
(1)如图所示为___(填“乙醇”或“乙酸”)的球棍模型。
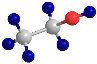
(2)乙醇中所含有的官能团的名称为___,乙酸中所含有的官能团的名称为___。
(3)写出实验室由乙醇制取乙醛的化学反应方程式___。
(4)写出如图所示装置中乙醇和乙酸反应的化学方程式:___。该反应的类型为___反应,右侧小试管中应装有___溶液。
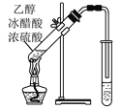
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 因为Na2CO3+SiO2![]() Na2SiO3+CO2↑,所以硅酸的酸性比碳酸强
Na2SiO3+CO2↑,所以硅酸的酸性比碳酸强
B. 碳和硅都是ⅣA族的元素,所以二氧化碳和二氧化硅的物理性质相似
C. 二氧化硅溶于氢氧化钠溶液又溶于氢氟酸,所以二氧化硅是两性氧化物
D. 二氧化硅和二氧化碳都是酸性氧化物,但二氧化硅不和水反应生成硅酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务。下列有关海水综合利用的说法不正确的是( )
A.从海水中提炼出的氘(含HDO 0.03‰)进行核聚变,放出巨大的能量以解决能源问题,成为一条新的科学思路,HDO与H2O化学性质相同
B.从海水中提取镁可以采用下列方法:海水![]() Mg(OH)2
Mg(OH)2![]() MgCl2溶液→MgCl2·6H2O
MgCl2溶液→MgCl2·6H2O![]() MgCl2(熔融)
MgCl2(熔融)![]() Mg[
Mg[
C.从海水获得的碘,可以跟氧气反应生成多种化合物,其中一种称为碘酸碘,在该化合物中,碘元素呈+3和+5两种价态,这种化合物的化学式是I4O9
D.除去粗盐中的SO42 -、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于A(g)+2B(g)![]() 3C(g)的化学反应,下列表示的反应速率最快的是( )
3C(g)的化学反应,下列表示的反应速率最快的是( )
A. v(A)=0.6 mol/(L·min) B. v(B)=0.3 mol/(L·s)
C. v(C)=0.9 mol/(L·min) D. v(C)=1.2 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库:从海水中提取食盐和溴的过程如下:
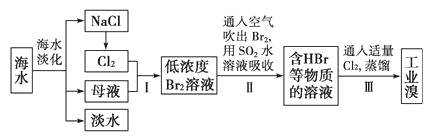
下列说法错误的是
A.海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等
B.电解熔融的氯化钠是一个将电能转化为化学能的过程
C.步骤Ⅱ中将Br2还原为Br-的目的是富集溴元素
D.向母液中加入石灰乳可得到Mg(OH)2,工业上常用电解熔融的Mg(OH)2来制取镁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com