
��10�֣���ijһ�ݻ�Ϊ5 L���ܱ������ڣ����� 0.3 mol��CO��0.3 mol��H2 O���ڴ������ں�800��������¼��ȣ��������·�Ӧ��CO(g)��H2O(g)
O���ڴ������ں�800��������¼��ȣ��������·�Ӧ��CO(g)��H2O(g) 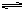 CO2(g)��H2(g)����Ӧ��CO2��Ũ����ʱ��仯�������ͼ��
CO2(g)��H2(g)����Ӧ��CO2��Ũ����ʱ��仯�������ͼ��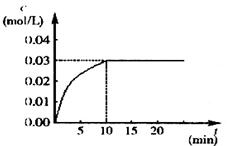
(1) ����ͼ�����ݣ���Ӧ��ʼ���ﵽƽ��ʱ��CO�Ļ�ѧ��Ӧ����Ϊv(CO)�� mol/(L��min)�����¶��µ�ƽ�ⳣ��K�� ��
(2) ������Ϊ�жϸ÷�Ӧ�ﵽƽ���������________________��(�����)
�� CO��H2O��CO2��H2��Ũ�ȶ���� �������淴Ӧ���ʶ�Ϊ��
�� CO��H2O��CO2��H2��Ũ�ȶ����ٷ����仯 �ܻ��������ܶȲ��ٷ����� ��
��
(3) ��Ҫһ��ʼ����0.1 mol��CO��0.1 mol��H2O��0.2 mol��CO2��0.2 mol��H2������ͬ�������£���Ӧ��ƽ��ʱ��c(CO)��________________mol/L��
(4) 427��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ9.4�����ϣ� 1���еļ������ش���������¶ȸ÷�Ӧƽ���� �����ƶ���
1���еļ������ش���������¶ȸ÷�Ӧƽ���� �����ƶ���

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ӧ��CO2��Ũ����ʱ��仯�������ͼ��
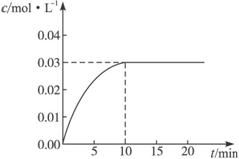
(1)������ͼ���ݣ���Ӧ��ʼ���ﵽƽ��ʱ��CO�Ļ�ѧ��Ӧ����Ϊ___________����Ӧ��ƽ��ʱ��c(H2)=______________��
(2)�жϸ÷�Ӧ�ﵽƽ���������_________��
��CO���ٵĻ�ѧ��Ӧ���ʺ�CO2���ٵĻ�ѧ��Ӧ�������
��CO��H2O��CO2��H2��Ũ�ȶ����
��CO��H2O��CO2��H2��Ũ�ȶ����ٷ����仯
�������淴Ӧ���ʶ�Ϊ��
(3)��Ҫһ��ʼ����0.1 mol��CO��0.1 mol��H2O��0.1 mol��CO2��0.1 mol��H2������ͬ�������£���Ӧ��ƽ��ʱ��c(H2O)=_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
![]() ��ijһ�ݻ�Ϊ5 L���ܱ������ڣ�����0��2 mol��CO��0��2 mol��H2O���ڴ������ڵ������¸��¼��ȣ��������·�Ӧ��CO��g��+H2O��g�� CO2��g��+H2��g������H��0��
��ijһ�ݻ�Ϊ5 L���ܱ������ڣ�����0��2 mol��CO��0��2 mol��H2O���ڴ������ڵ������¸��¼��ȣ��������·�Ӧ��CO��g��+H2O��g�� CO2��g��+H2��g������H��0��
��Ӧ��CO2��Ũ����ʱ��仯�������ͼ��
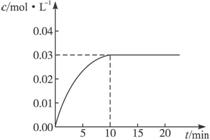
��1��������ͼ���ݣ���Ӧ��ʼ���ﵽƽ��ʱ��CO�Ļ�ѧ��Ӧ����Ϊ___________����Ӧ��ƽ��ʱ��c��H2��=______________��
��2���жϸ÷�Ӧ�ﵽƽ���������_________��
��CO���ٵĻ�ѧ��Ӧ���ʺ�CO2���ٵĻ�ѧ��Ӧ�������
��CO��H2O��CO2��H2��Ũ�ȶ����k+s-5#u ![]()
��CO��H2O��CO2��H2��Ũ�ȶ����ٷ����仯
�������淴Ӧ���ʶ�Ϊ��
��3����Ҫһ��ʼ����0��1 mol��CO��0��1 mol��H2O��0��1 mol��CO2��0��1 mol��H2������ͬ�������£���Ӧ��ƽ��ʱ��c��H2O��=_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ijһ�ݻ�Ϊ5 L���ܱ������ڣ�����0.2 mol CO��0.2 mol H2O���ڴ������ڵ������¸��¼��ȣ��������·�Ӧ��CO��g��+H2O��g��![]() CO2��g��+H2��g�� ��H��0����Ӧ��CO2��Ũ����ʱ��仯�����ͼ��ʾ��
CO2��g��+H2��g�� ��H��0����Ӧ��CO2��Ũ����ʱ��仯�����ͼ��ʾ��
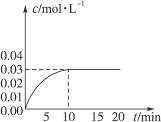
��1������ͼ�����ݣ���Ӧ��ʼ���ﵽƽ��ʱ��CO�Ļ�ѧ��Ӧ����Ϊ__________����Ӧ��ƽ��ʱ��c��H2����__________��
��2���жϸ÷�Ӧ��ƽ���������__________������ţ���
��CO���ٵ����ʺ�CO2���ٵ��������
�� CO��H2O��CO2��H2��Ũ�ȶ����
��CO��H2O��CO2��H2��Ũ�ȶ����ٷ����仯
�ܸ������������淴Ӧ���ʶ�Ϊ��
��3�����һ��ʼ����0.1 mol��CO��0.1 mol��H2O��0.1 mol��CO2��0.1 mol��H2������ͬ�����£���Ӧ��ƽ��ʱ��c��H2O����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ����������һ�и߶���ѧ����ĩ���Ի�ѧ�Ծ����������� ���ͣ������
��ijһ�ݻ�Ϊ5 L���ܱ������ڣ�����0.3 mol��CO��0.3 mol��H2O���ڴ������ں�800��������¼��ȣ��������·�Ӧ��CO(g)��H2O(g) 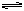 CO2(g)��H2(g) ��H>0����Ӧ��CO2��Ũ����ʱ��仯�������ͼ��
CO2(g)��H2(g) ��H>0����Ӧ��CO2��Ũ����ʱ��仯�������ͼ��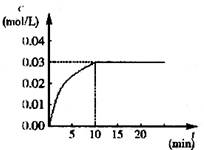
(1)����ͼ�����ݣ���Ӧ��ʼ���ﵽƽ��ʱ��
CO�Ļ�ѧ��Ӧ����Ϊv(CO)�� mol/(L��min)-1��
���¶��µ�ƽ�ⳣ��K�� ��
(2)���������������£��ı������������´ﵽƽ��ʱ��ʹƽ�ⳣ��K�������
������ĸ��
| A�������¶� | B�������¶� | C������ѹǿ | D����Сѹǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�����ĸ߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
��ijһ�ݻ�Ϊ5 L���ܱ������ڣ�����0.3 mol��CO��0.3 mol��H2O���ڴ������ں�800��������¼��ȣ��������·�Ӧ��CO(g)��H2O(g) 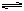 CO2(g)��H2(g)
��H>0����Ӧ��CO2��Ũ����ʱ��仯�������ͼ��
CO2(g)��H2(g)
��H>0����Ӧ��CO2��Ũ����ʱ��仯�������ͼ��
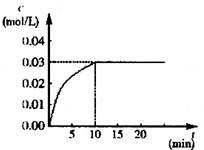
(1)����ͼ�����ݣ���Ӧ��ʼ���ﵽƽ��ʱ��
CO�Ļ�ѧ��Ӧ����Ϊv(CO)�� mol/(L��min)-1��
���¶��µ�ƽ�ⳣ��K�� ��
(2)���������������£��ı������������´ﵽƽ��ʱ��ʹƽ�ⳣ��K�������
������ĸ��
A�������¶� B�������¶� C������ѹǿ D����Сѹǿ
E��������� G���Ƴ�һ����̼����
(3)��Ҫһ��ʼ����0.1 mol��CO��0.1 mol��H2O��0.2 mol��CO2��0.2 mol��H2������ͬ�������£���Ӧ��ƽ��ʱ��c(CO)��________________mol/L.
(4)�������¶Ⱥ�������������䣬��(1)������ƽ����ϵ�У��ٳ���0.3mol ��ˮ���������´ﵽƽ���CO��ת����_______(����ߡ��������͡����ǡ����䡱)��CO2����������________(����ߡ��������͡����ǡ����䡱).
(5)�ڴ������ں�800��������£���ijһʱ�̲��C(CO)=C(H2O)= 0.09mol/L,
C(CO2 )=C(H2)=0.13mol/L ,��˷�Ӧ�Ƿ���ƽ��״̬: (��ǡ���),��û�д���ƽ��״̬��÷�Ӧ�� �ƶ�������������淽��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com