
【题目】NA表示阿伏加德罗常数的值。下列说法正确的是
A. 一定条件下,1molN2和3molH2混合后,反应转移的电子数目为6NA
B. 1.0L0.1mol/LNa2S溶液中含有的S2-数为0.1NA
C. 1molCu与含2molH2SO4的浓硫酸充分反应,生成的SO2的分子个数为NA
D. 向含有FeI2的溶液中通入适量氧气,当有1molFe2+被氧化时,该反应转移的电子数目至少为3NA
【答案】D
【解析】A. 一定条件下,氮气和氢气合成氨是可逆反应,故1molN2和3molH2混合后,反应转移的电子数目小于6NA,选项A错误;B、S2-为弱酸根,在溶液中会水解,故溶液中的硫离子的个数小于0.1NA个,选项B错误;C、根据化学方程式Cu+2H2SO4![]() CuSO4+SO2↑+2H2O,可知1mol铜与2mol硫酸恰好反应,但随着反应的进行,浓硫酸浓度变稀,所以当浓度到一定程度时,铜不再和稀硫酸反应,因此实际生成的二氧化硫气体应小于1mol,即NA,选项D错误;D、向FeI2溶液中通入足量氯气,I->Fe2+,当有1mol Fe2+被氧化时,2mol碘离子全部被氧化,电子转移数目3NA,选项D正确;答案选D。
CuSO4+SO2↑+2H2O,可知1mol铜与2mol硫酸恰好反应,但随着反应的进行,浓硫酸浓度变稀,所以当浓度到一定程度时,铜不再和稀硫酸反应,因此实际生成的二氧化硫气体应小于1mol,即NA,选项D错误;D、向FeI2溶液中通入足量氯气,I->Fe2+,当有1mol Fe2+被氧化时,2mol碘离子全部被氧化,电子转移数目3NA,选项D正确;答案选D。


科目:高中化学 来源: 题型:
【题目】在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件关于离子共存说法中正确的是( )
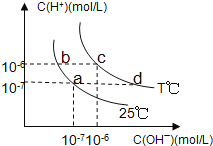
A. a点对应的溶液中大量存在:Fe3+、Na+、Cl―、SO42―
B. b点对应的溶液中大量存在:NH4+、Ba2+、OH―、I―
C. c点对应的溶液中大量存在:Na+、Ba2+、Cl―、HCO3―
D. d点对应的溶液中大量存在:Na+、K+、SO32―、Cl―
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组的同学欲利用下图所示的装置验证浓硝酸与木碳反应时有NO2、CO2生成,探究是否还有NO生成。已知二氧化氮易液化(沸点为21.1℃),而NO、CO2难液化。
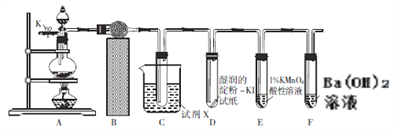
(1)装置连接好后,首先要进行的操作是_________;然后打开开关K,通过导管向装置内通入N2的目的是_________。
(2)B中的试剂是_________,C是用于检验NO2的,试剂X最好是_________(填“水”或“冰水”),D的作用是_________。
(3)若将装置C改为盛有淀粉-KI溶液的试管,也能确定有NO2生成,实验中不用此种方法的原因是_________________;假设E中溶液的颜色慢慢褪去,则E中最可能发生的反应的离子方程式为_________________;若E中没有明显的变化,C、F中出现了预期的现象,则A中反应的化学方程式为_________________。
(4)将等物质的量的NO2、NO通入冰冻的水中只可得到一种比碳酸酸性强的酸,该酸的化学式为_________,设计一种实验方案证明其酸性比碳酸的酸性强_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
A. 放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B. 充电时阳极反应为:Fe(OH)3-3e-+5OH-=![]() +4H2O
+4H2O
C. 放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两种金属混合物3.4g,与足量的盐酸反应放出H22.24L(标况下),这两种金属可能是
A. 铜和铁 B. 镁和铝 C. 锌和铝 D. 锌和铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。

回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为________________ 、_______________ ;
(2)闭合K开关后,a、b电极上均有气体产生.其中a电极上得到的是_________(填化学式),电解氯化钠溶液的总反应方程式为___________________;
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上最多能产生的氯气体积为____________L(标准状况);
(4)若饱和氯化钠溶液体积为100mL,电解一段时间后,常温下测得溶液pH为13,若要使溶液恢复到电解前的状态,可向溶液中加(或通)入__________(填写物质的化学式)_________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛分子的结构式如图所示,下列描述正确的是( )
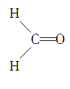
A. 甲醛分子中有4个σ键
B. 甲醛分子中的C原子为sp3杂化
C. 甲醛分子中的O原子为sp杂化
D. 甲醛分子为平面三角形,有一个π键垂直于三角形平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:
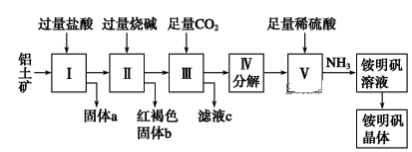
请回答下列问题:
(1)固体a的化学式为________。
(2)写出Ⅱ中加过量的烧碱涉及到的反应离子方程式______________、_____________;Ⅲ中通入足量CO2气体发生反应的离子方程式为_______________。
(3)由Ⅲ中得到滤液c的实验操作为__________,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)________、冷却结晶、过滤洗涤。
(4)将NH4Al(SO4)2溶液和Ba(OH)2溶液,按物质的量比1:2混合,写出离子方程式为_______________。
(5)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠和碳酸氢钠是生活中常见的物质,请回答下列问题。
(1)碳酸氢钠的俗称是_________,其水溶液显_____性。(填“酸”、“碱”或“中”)。
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式____________。等物质的量的碳酸钠和碳酸氢钠分别与足量盐酸反应时生成CO2的量,前者________后者(填“>”、“<”或“=”)。
(3)除去碳酸钠固体中碳酸氢钠的反应的化学方程式为________________________________。
(4)硫酸亚铁是缺铁性贫血的治疗药物,可用于制备铁盐,实验室检验Fe3+的方法是:向溶液中滴入几滴_________________溶液,观察溶液是否变为血红色。向FeSO4溶液中加入NaOH溶液通常得不到白色的Fe(OH)2沉淀,其原因是_________________________(用化学方程式回答)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com