
【题目】图 1 是课本“还原铁粉与水蒸气反应”的实验装置图。
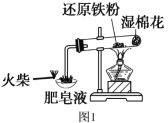
(1)写出铁粉与水蒸气反应的化学方程式,并用“单线桥”标出电子转移方向及数目 :_____________;其中氧化剂为________________(写化学式);标况下,生成气体2.24L,则消耗Fe的质量为__________g。
(2)证明还原铁粉与水蒸气发生了反应的现象是: ________________。 若将反应生成的固体产物溶于盐酸,其离子反应方程式为________________。
【答案】![]() H2O 4.2 肥皂泡上升,点燃有爆鸣声 Fe3O4 + 8H+ = Fe2+ + 2Fe3+ + 4H2O
H2O 4.2 肥皂泡上升,点燃有爆鸣声 Fe3O4 + 8H+ = Fe2+ + 2Fe3+ + 4H2O
【解析】
(1)Fe与水蒸气高温下反应生成四氧化三铁和氢气,转移8e-,结合氧化还原反应的规律分析解答;
(2)氢气具有可燃性,四氧化三铁与盐酸反应生成氯化铁、氯化亚铁、水,据此分析解答。
(1)Fe与水蒸气高温下反应生成四氧化三铁和氢气,转移8e-,反应及电子转移方向及数目可以表示为![]() ,H元素的化合价降低,则H2O为氧化剂,生成4mol气体时消耗3molFe,则标况下,生成气体2.24L,则消耗Fe的质量为
,H元素的化合价降低,则H2O为氧化剂,生成4mol气体时消耗3molFe,则标况下,生成气体2.24L,则消耗Fe的质量为![]() ×
×![]() ×56g/mol=4.2g,故答案为:
×56g/mol=4.2g,故答案为:![]() ;H2O;4.2;
;H2O;4.2;
(2)还原铁粉与水蒸气发生了反应的现象是肥皂泡上升,点燃有爆鸣声,将反应生成的固体产物溶于盐酸,其离子反应方程式为Fe3O4+8H+=Fe2++2Fe3++4H2O,故答案为:肥皂泡上升,点燃有爆鸣声;Fe3O4+8H+=Fe2++2Fe3++4H2O。


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
【题目】碱式氯化铜[CuaClb(OH)c·xH2O]是一种重要的无机杀虫剂,它可以通过以下步骤制备。步骤1:将铜粉加入稀盐酸中,并持续通空气反应生成CuCl2。已知Fe3+对该反应有催化作用,其催化原理如下图所示。步骤2:在制得的CuCl2溶液中,加入石灰乳充分反应后即可制备碱式氯化铜。
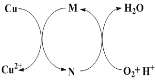
下列有关说法正确的是
A. a、b、c 之间的关系式为:a=b+c
B. 图中M、N分别为Fe2+、Fe3+
C. 步骤1充分反应后,加入少量CuO是为了除去Fe3+
D. 若制备1 mol的CuCl2,理论上消耗11.2 LO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“钙基固硫”是将煤中的硫元素以CaSO4的形式固定脱硫,而煤炭燃烧过程中产生的CO又会发生反应I和反应II,导致脱硫效率降低。某温度下,反应I的速率(v1)大于反应II的速率(v2),则下列反应过程能量变化示意图正确的是
反应I:CaSO4(s)+CO(g) ![]() CaO(s)+SO2(g)+CO2(g) △H1=+218.4kJ·mol-1
CaO(s)+SO2(g)+CO2(g) △H1=+218.4kJ·mol-1
反应II:CaSO4(s)+4CO(g) ![]() CaS(s)+4CO2(g) △H2=-175.6kJ·mol-1
CaS(s)+4CO2(g) △H2=-175.6kJ·mol-1

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NOx、CO等大气污染气体的处理,对保护环境有重要的意义。回答下列问题:
(1)NOx与CO反应生成无污染气体的相关热化学方程式如下:①NO2(g)+CO(g)![]() CO2(g)+NO(g) ΔH1=234.0 kJ·mol1,②N2(g) +O2(g)
CO2(g)+NO(g) ΔH1=234.0 kJ·mol1,②N2(g) +O2(g)![]() 2NO(g)ΔH2=+179.5 kJ·mol1,③2NO(g)+O2(g)
2NO(g)ΔH2=+179.5 kJ·mol1,③2NO(g)+O2(g)![]() 2NO2(g) ΔH3=112.3 kJ·mol1,反应2NO2(g) +4CO(g)
2NO2(g) ΔH3=112.3 kJ·mol1,反应2NO2(g) +4CO(g)![]() N2(g)+4CO2(g)的ΔH=__________ kJ·mol1。
N2(g)+4CO2(g)的ΔH=__________ kJ·mol1。
(2)在一定温度下,向2 L的恒容密闭容器中充入4.0 mol NO2和4.0 mol CO,在催化剂作用下发生反应:2NO2(g)+4CO(g)![]() N2(g) +4CO2(g),测得相关数据如下:
N2(g) +4CO2(g),测得相关数据如下:
0 min | 5 min | 10 min | 15 min | 20 min | |
c(NO2)/mol·L1 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
c(N2)/mol·L1 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
①在0~10 min,用CO2的浓度变化表示的反应速率为______________。
②为使该反应的反应速率增大,下列措施中可采用的是________(填字母代号)。
a.减小压强 b.适当升高温度 c.增大CO的浓度 d.选择高效催化剂
(3)如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
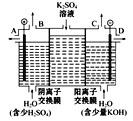
①该电解槽的阳极反应式为_______。此时通过阴离子交换膜的离子数____(填“大于”“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口____(填“A”“B”“C”或“D”)导出。
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池负极的电极反应式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)具有复合官能团的复杂有机物,其官能团具有各自的独立性,在不同条件下所具有的化学性质可分别从各官能团讨论。如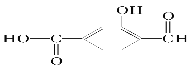 具有三种官能团:______、__________和__________(填官能团的名称),所以这个化合物可看作______类,______类和______类。
具有三种官能团:______、__________和__________(填官能团的名称),所以这个化合物可看作______类,______类和______类。
(2)羟基的电子式是___________________________。
(3)(CH3CH2)2C(CH3)2的名称为_________________________。
(4)2-甲基-1,3-丁二烯的键线式___________________________。
(5)![]() 该有机物发生加聚反应后,所得产物的结构简为______。
该有机物发生加聚反应后,所得产物的结构简为______。
(6)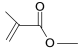 分子式为_______________________结构简式为______________________。
分子式为_______________________结构简式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硫酰氯(俗称氯化亚砜,SOCl2)是一种液态化合物,沸点77℃,在农药、制药行业、有机合成等领域用途广泛。SOCl2遇水剧烈反应,液面上产生白雾,并常有刺激性气味的气体产生,实验室合成原理:SO2+Cl2+SCl2=2SOCl2,部分装置如图所示:
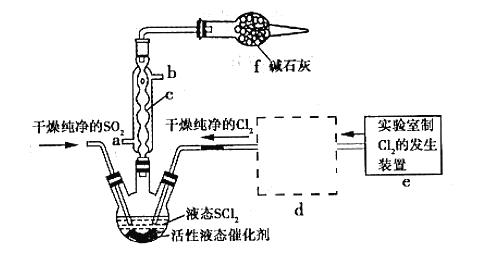
请回答下列问题:
(1)装置f的作用是____________
(2)实验室用二氧化锰与浓盐酸共热反应的离子方程式为____________。
(3)蒸干AlCl3溶液不能得到无水AlCl3,使SOCl2与AlCl3·6H2O混合加热,可得到无水AlCl3,试解释原因:_______________________________________________________
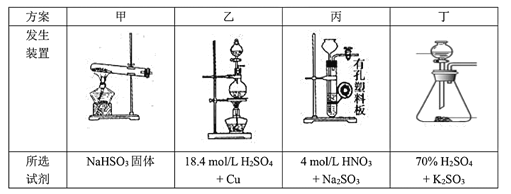
(4)下列四种制备SO2的方案中最佳选择是____。
(5)装置e中产生的Cl2经过装置d后进入三颈烧瓶, d中所用的试剂为_______。(按气流方向)
(6)实验结束后,将三颈烧瓶中混合物分离开的实验操作是________(己知SCl2的沸点为50℃)。若反应中消耗Cl2的体积为896 mL(己转化为标准状况,SO2足量),最后得到纯净的SOCl2 4.76 g,则SOCl2的产率为__________(保留三位有效数字)。
(7)分离产物后,向获得的SOCl2中加入足量NaOH溶液,振荡、静置得到无色溶液W,检验溶液W中存在Cl-的方法是_______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同质量的SO2和SO3,它们之间的关系正确的是
A.所含硫原子的物质的量之比为1:1
B.所含硫元素的质量比为5:4
C.所含氧元素的质量比为4:5
D.所含氧原子的物质的量之比为3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,8.8mgCO2通过一定量的Na2O2固体后,最终收集到3.36mL气体,则这3.36mL气体的成分是( )
A.CO2B.CO2和O2C.O2D.无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com