
【题目】化工厂生产盐酸的主要过程是:


其中关键的一步为如图所示的氯气和氢气在燃烧管口燃烧生成HCl。氯气有毒,为此通人气体的合理方式是:
(1)A处通入_____,B处通入_____,同时应采取的措施是____。
(2)合成盐酸厂要求合成气中的HCl的含量要大于97%,试用最简便的方法进行分析是否含量大于97%_____。
【答案】H2 Cl2 通入过量的H2 用一个100mL有刻度的容器收集满该合成气体倒置于水中,如水沿器壁上升到97mL刻度以上。
【解析】
(1)根据氯气有毒,通入的氢气应该是过量的,为防止污染空气,应该先通氢气,在通氯气等知识进行分析;
(2)根据氯化氢易溶于水进行分析。
(1)氯气有毒,通入的氢气应该是过量的,为防止污染空气,应该先通氢气,在通氯气,所以A处通入氢气,B处通入氯气,采取的措施是:先通氢气点燃,再通氯气;
(2)氯化氢易溶于水,所以验证的方法是:用一个100mL有刻度的容器收集满该合成气体倒置于水中,如水沿器壁上升到97mL刻度以上,即说明合成气中的HCl的含量大于97%。


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
【题目】下列关于0.10 mol·L-1 NaHCO3溶液的说法正确的是( )
A. 溶质的电离方程式为NaHCO3===Na++H++CO![]()
B. 25 ℃时,加水稀释后,n(H+)与n(OH-)的乘积变大
C. 离子浓度关系:c(Na+)+c(H+)=c(OH-)+c(HCO![]() )+c(CO
)+c(CO![]() )
)
D. 温度升高,c(HCO![]() )增大
)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关一定物质的量浓度溶液的配制说法中正确的是( )
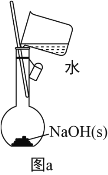
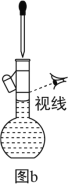
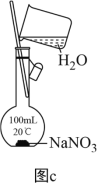
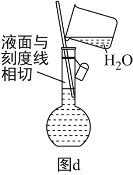
(1)为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至接近刻度线时,改用胶头滴管滴加蒸馏水至刻度线
(2)利用图a配制0.10molL-1NaOH 溶液
(3)利用图b配制一定浓度的NaCl溶液
(4)利用图c配制一定物质的量浓度的NaNO3溶液
(5)用容量瓶配制溶液时,若加水超过刻度线,立即用滴管吸出多余液体
(6)配制溶液的定容操作可以用图d表示
A. (2)(5)B. (1)(4)(6)
C. (1)D. (1)(3)(5)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了如下实验检验某溶液中是否含有SO42—:
溶液![]() 白色沉淀
白色沉淀![]() 白色沉淀不溶解
白色沉淀不溶解
结论:溶液中有SO42—。
(1)该方案是否严密?________。
(2)请说明理由:_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关图像的叙述正确的是
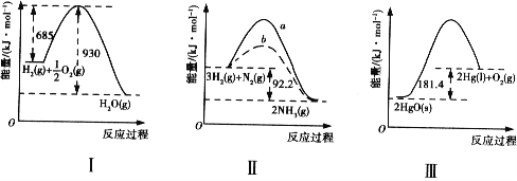
A. 图 I:H2 的燃烧热为 245 kJ/mol
B. 图 II:b 可能为使用催化剂的曲线,活化能降低
C. 图 II:向容器中充入 1 mol N2、3 mol H2,充分反应后放出热量 92.2 kJ
D. 图 III:HgO(s) = Hg(l) + 1/2O2(g) △H = - 90.7 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】13C-NMR(核磁共振)可用于含碳化合物的结构分析,15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下面有关13C、15N的叙述正确的是( )
A.13C与15N具有相同的中子数B.13C与C60是同一种物质
C.15N与14N互为同位素D.15N的核外电子数与中子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:(1)实验室制取Cl2的方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,其中MnO2发生了__反应,是__剂;每4分子氯化氢中只有___分子发生了___反应,盐酸是___剂。
MnCl2+Cl2↑+2H2O,其中MnO2发生了__反应,是__剂;每4分子氯化氢中只有___分子发生了___反应,盐酸是___剂。
(2)室温下KMnO4与浓盐酸反应制取氯气的化学方程式:2KMnO4+16HCl(浓)===2KCl+2MnCl2+8H2O+5Cl2↑,请在上式中用单线桥法表示出不同元素的原子间得失电子的情况。___
(3)用CuCl2作催化剂,在450℃时用空气中的O2跟HCl反应也能制得氯气,其化学方程式:4HCl+O2![]() 2H2O+2Cl2,从氯元素化合价的变化看,以上三种制氯气方法的共同点是__;比较以上三个反应,可以认为氧化剂的氧化能力从强到弱的顺序为___。
2H2O+2Cl2,从氯元素化合价的变化看,以上三种制氯气方法的共同点是__;比较以上三个反应,可以认为氧化剂的氧化能力从强到弱的顺序为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①Fe+H2SO4(稀)=FeSO4+H2↑
②Cu+2H2SO4(浓) ![]() CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑
③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
试回答下列问题:
(1)当反应①转移3摩尔电子时,消耗H2SO4的质量是______g,产生氢气的体积(标准状况)_________L。
(2)反应②中_________作氧化剂,___________是氧化产物。
(3)当反应②中生成11.2LSO2气体(标准状况下)时,被还原的H2SO4的物质的量是____________。
(4)用单线桥法表示反应②电子转移的方向和数目(在化学方程式上标出)。___________
Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑
(5)反应③中氧化产物与还原产物的物质的量之比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属(Ti)是航空、宇航、军工、电子等方面的必需原料。在生产钛的过程中可用镁在加热条件下与TiCl4反应制得金属钛,反应的化学方程式为:TiCl4+2Mg![]() Ti+2MgCl2。该反应属于( )
Ti+2MgCl2。该反应属于( )
A. 化合反应B. 分解反应C. 置换反应D. 无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com