
 3Fe2+
3Fe2+ 2H2O+2Fe3+
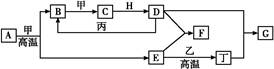
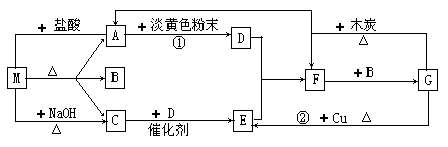
2H2O+2Fe3+ 丁(单质)可知,丁为Fe,D(H2SO4)+E(Fe2O3)
丁(单质)可知,丁为Fe,D(H2SO4)+E(Fe2O3) F,则F为Fe2(SO4)3。(1)FeS2高温下燃烧的化学方程式为:4FeS2+11O2
F,则F为Fe2(SO4)3。(1)FeS2高温下燃烧的化学方程式为:4FeS2+11O2 2Fe2O3+8SO2,由此分析可知,每消耗4 mol FeS2,转移电子为44 mol,即每反应1 mol的A(FeS2)转移的电子为11 mol;(2)由转化关系图可知F为Fe2(SO4)3,丁为Fe,G为FeSO4,则有关的离子反应为Fe+2Fe3+
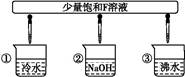
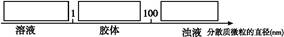
2Fe2O3+8SO2,由此分析可知,每消耗4 mol FeS2,转移电子为44 mol,即每反应1 mol的A(FeS2)转移的电子为11 mol;(2)由转化关系图可知F为Fe2(SO4)3,丁为Fe,G为FeSO4,则有关的离子反应为Fe+2Fe3+ 3Fe2+;(3)将少量饱和Fe2(SO4)3溶液加入①冷水中形成溶液;加入②NaOH溶液中会产生Fe(OH)3沉淀,形成浊液;加入③沸水中会产生Fe(OH)3胶体;(4)化合物M与H(H2O)组成元素相同,则M为H2O2,M在酸性条件下将G(FeSO4)氧化为F[Fe2(SO4)3]的离子方程式为:H2O2+2H++2Fe2+
3Fe2+;(3)将少量饱和Fe2(SO4)3溶液加入①冷水中形成溶液;加入②NaOH溶液中会产生Fe(OH)3沉淀,形成浊液;加入③沸水中会产生Fe(OH)3胶体;(4)化合物M与H(H2O)组成元素相同,则M为H2O2,M在酸性条件下将G(FeSO4)氧化为F[Fe2(SO4)3]的离子方程式为:H2O2+2H++2Fe2+ 2H2O+2Fe3+。
2H2O+2Fe3+。

科目:高中化学 来源:不详 题型:填空题
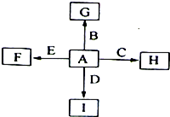
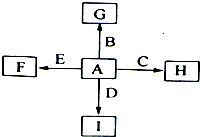
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 ,下列说法不正确是
,下列说法不正确是| A.①③ | B.②③ | C.②③④ | D.全部 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.第二周期元素从C到F,非金属性逐渐减弱 |
| B.第三周期元素从Na到Cl,原子半径逐渐增大 |
| C.HF、HCl、HBr、HI的热稳定性依次逐渐减弱 |
| D.LiOH、NaOH、KOH的碱性依次逐渐减弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com