
| A. | 标准状况下,22.4L H2O的分子数为 NA | |
| B. | 常温常压下,1mol甲基(-CH3)所含的电子数为10NA | |
| C. | 2.3g金属钠反应生成Na2O2时失去的电子数为0.1NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA |
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②两个反应互为可逆反应 | B. | ①②两反应都是放热反应 | ||
| C. | ②反应是热能转变为化学能 | D. | ①反应是热能转变为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2OH→CH2=CH2↑+H2O | B. | 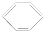 +Br2→ +Br2→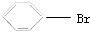 +HBr +HBr | ||
| C. | CH3CHO+H2→CH3CH2OH | D. | CH4+2O2→CO2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 配料 | 氯化钠、碘酸钾 |
| 含碘量 | (40~50)mg/kg(以I计) |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮藏指南 | 避热、避光、密封、防潮 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入足量SO2的溶液中:Fe2+、Na+、SO42-、ClO- | |
| B. | 常温下,c(H+)═$\sqrt{{K}_{w}}$的溶液中:Na+、Fe3+、HCO3-、K+ | |
| C. | 水电离出的c(OH-)=10-13 mol/L的溶液中:Ba2+、Cl-、NO3-、I- | |
| D. | 遇酚酞显红色的溶液中:AlO2-、HCO3-、K+、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 便于消防人员快速通行 | B. | 将可燃物与火源隔离 | ||
| C. | 减少可燃物与空气的接触面积 | D. | 降低可燃物的着火点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.8g | B. | 4.4g | ||
| C. | 5.6g | D. | 在2.8g和5.6g之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
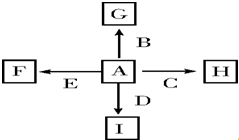 图中A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.
图中A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com