
(8分)(1)已知H2(g)燃烧热为-285.8kJ·mol-1用太阳能分解10mol水消耗的能量是_____________kJ;
(2)已知0.4 mol液态肼(N2 H4)与足量H2O2反应,生成氮气和水蒸气,放出256.65 kJ的热量。写出该该反应的热化学方程式__________________________________________________。
又已知 H2O(l)=== H2O(g)ΔH=+44kJ·mol-1则16g液态肼与足量H2O2反应,生成氮气和液态水放出的热量是_____________ kJ。
上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是____________________________________________________________。
(8分,每空2分)(1)2858
(2)N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) △H=—641.625kJ/mol
408.8 生成的N2和 H2O,对环境无污染。
【解析】(1)H2(g)燃烧热为-285.8kJ·mol-1,这说明分解1mol水需要消耗285.8kJ能量,所以用太阳能分解10mol水消耗的能量是285.8kJ×10=2858kJ。
(2).4 mol液态肼(N2 H4)与足量H2O2反应,生成氮气和水蒸气,放出256.65 kJ的热量。
则1mol液态肼完全燃烧放出的能量是256.65 kJ×1mol÷0.4mol=641.625kJ,所以热化学方程式为N2H4(l)+2H2O2(l)=N2(g)+4H2O(g) △H=—641.625kJ/mol。16g液态肼是0.5mol,完全燃烧生成2mol水蒸气放出热量是641.625kJ÷2=320.8125kJ。其中2mol水蒸气变成液态水有放出44kJ×2=88kJ,所以最终放出的热量是320.8125kJ+88kJ=408.8kJ。根据方程式可知,生成物是N2和 H2O,对环境无污染。


科目:高中化学 来源: 题型:
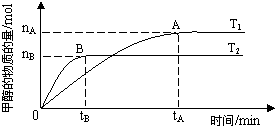 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.| nA |
| tA |
| nA |
| tA |
| a |
| 2 |
| a |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省永城实验高中高二上学期期中考试化学试卷(带解析) 题型:填空题
(8分)(1)已知H2(g)燃烧热为-285.8kJ·mol-1用太阳能分解10mol水消耗的能量是_____________kJ;
(2)已知0.4 mol液态肼(N2 H4)与足量H2O2反应,生成氮气和水蒸气,放出256.65 kJ的热量。写出该该反应的热化学方程式__________________________________________________。
又已知 H2O(l)=== H2O(g)ΔH=+44kJ·mol-1则16g液态肼与足量H2O2反应,生成氮气和液态水放出的热量是_____________ kJ。
上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山西省忻州市原平一中高二(上)期中化学试卷(普通班)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com