
【题目】在一定温度下的恒容容器中,当下列物理量不再发生变化时:①混合气体的压强;②混合气体的密度;③混合气体的总物质的量;④混合气体的平均相对分子质量;⑤混合气体的颜色;⑥各反应物或生成物的浓度之比等于化学计量数之比;⑦某种气体的百分含量。能说明A(s)![]() 3B(g)+C(g)达到平衡状态的是( )
3B(g)+C(g)达到平衡状态的是( )
A. ①②③④
B. ①②③④⑦
C. ①③④⑦
D. ①②③
【答案】D
【解析】
①该反应是反应前后气体体积不等的反应,若混合气体的压强不变,则反应达到平衡状态,①正确;
②该反应反应前后气体的质量变化,容器的容积不变,所以混合气体的密度不变,反应达到平衡状态,②正确;
③反应物不是气体,生成物是气体,若混合气体的总物质的量不变,则反应达到平衡状态,③正确;
④只有生成物是气体,二者的物质的量的比始终不变,因此混合气体的平均相对分子质量总是不变,因此不能据此判断反应是否处于平衡状态,④错误;
⑤题干未指明气体有颜色,因此不能根据混合气体的颜色变化判断平衡状态,⑤错误;
⑥反应物是固体,浓度不变,而生成物中任何情况下生成物的浓度之比等于化学计量数之比,不能据此判断为平衡状态,⑥错误;
⑦只有生成物为气体,二者的含量始终不变,因此不能根据某种气体的百分含量不变判断反应是否处于平衡状态,⑦错误;
故能说明A(s)![]() 3B(g)+C(g)达到平衡状态的是①②③,含量选项是D。
3B(g)+C(g)达到平衡状态的是①②③,含量选项是D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:
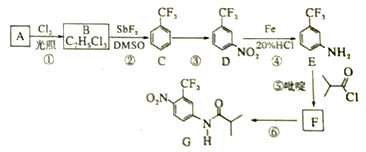
回答下列问题:
(1)A的结构简式为_______________。C的化学名称是________________________。
(2)③的反应试剂和反应条件分别是______________________,该反应的类型是___________。
(3)⑤的反应方程式为_____________________________________________。
吡啶是一种有机碱,其作用是______________________________。
(4)G的分子式为______________________________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则Ⅱ可能的结构有_________种。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )制备小甲氧基乙酸苯胺的合成路线(其他试剂任选)_______________。
)制备小甲氧基乙酸苯胺的合成路线(其他试剂任选)_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种物质是含钠元素的单质或化合物,其中A为银白色固体,B为淡黄色固体,它们有如图所示的转化关系:
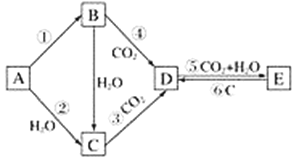
(1)推断各符号所代表的物质的化学式:
A________________,B________________,C________________,D________________,E________________。
(2)分别写出反应②⑤的化学方程式:
②________________________________________________________________________;
⑤________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的常用试剂是___,证明Fe3+存在的现象是____,配制含Fe2+的溶液时,常常向溶液中加入少量___,使被氧气氧化形成的Fe3+还原为Fe2+。
(2)写出FeCl3溶液与金属铜发生反应的化学方程式:___。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:
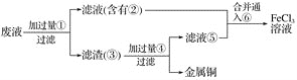
A.请写出上述实验中加入或生成的有关物质的化学式。
①___,②___,③___,④____,⑤____,⑥_____。
B.请写出相关反应的化学方程式。_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铝合金(硬铝)中含有镁、铜、硅,为了测定该合金中铝的含量,有人设计如下实验:
(1)称取样品ag。
(2)将样品溶于足量稀盐酸中,过滤,滤液中主要含有___离子,滤渣中含有___;在溶解过滤时使用的仪器有___。
(3)往滤液中加入过量NaOH溶液,过滤,写出该步操作中有关的离子方程式____。
(4)在第(3)步的滤液中通入足量CO2过滤,将沉淀用蒸馏水洗涤数次后,烘干并灼烧至质量不再减少为止,冷却后称量,质量为bg。有关反应的化学方程式为____。
(5)计算该样品中铝的质量分数的表达式为___。
(6)若第(3)步中加入NaOH溶液的量不足时,会使测定的结果___(“偏高”“偏低”或“无影响”,下同)。若第(4)步对沉淀的灼烧不充分时,会使测定的结果___。若第(4)步中的沉淀没有用蒸馏水洗涤时,会使测定的结果____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法,正确的是( )
A.由甲烷在纯氧中完全燃烧只生成CO2和H2O说明甲烷不含氧元素
B.![]() 最多有16个原子共平面
最多有16个原子共平面
C.油脂在人体内水解为氨基酸和甘油等小分子才能被吸收
D.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度和压强下,对反应X(g)+Y(g)![]() Z(g)+W(g)进行四组实验,实验起始时放入容器内各组分的物质的量见表:
Z(g)+W(g)进行四组实验,实验起始时放入容器内各组分的物质的量见表:
实验 | X | Y | Z | W |
① | amol | amol | 0mol | 0mol |
② | 3amol | amol | 0mol | 0mol |
③ | 0mol | 0mol | amol | amol |
④ | 2amol | 0mol | amol | amol |
上述四种情况达到平衡后,n(Z)的大小顺序是( )
A. ②=④>①=③B. ②>④>①>③
C. ④>②>①=③D. ④>③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4,二元弱酸)与草酸盐在实验和工业生产中都起着重要的作用,常温下,H2C2O4:Ka1=5.4×10-2,Ka2=5.4×10-5。H2CO3:K1=4×10-7K2=6×10-11。
(1)NaHCO3溶液显____性。
(2)常温下,0.1mol·L-1的Na2C2O4溶液pH=a,0.1 mol·L-1的Na2CO3溶液pH=b,则a___b(填“>”“<”或“=”)。
(3)常温下,pH=3的H2C2O4溶液的物质的量浓度为c1,水电离出的c(H+)为c3;pH=4的H2C2O4溶液的物质的量浓度为c2,水电离出的c(H+)为c4。则c1_____10c2(填“>”“<”或“=”,下同);c3___10c4。
(4)常温下,用0.1000mol·L-1NaOH溶液滴定20.00mL某未知浓度的H2C2O4溶液,滴定曲线如图,c点所示溶液中:2c(C2O42-)+2c(HC2O4-)+2c(H2C2O4)=c(Na+)
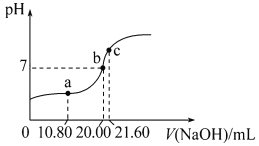
①该草酸溶液的物质的量浓度为_________(结果保留三位小数)。
②a点所示溶液中各离子的浓度由大到小的顺序为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为地壳中含量最多的金属元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。
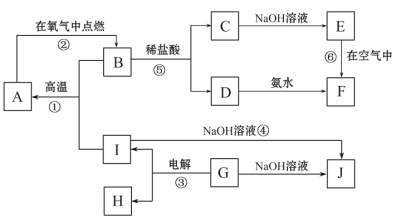
请填写下列空白:
(1)写出下列物质的化学式A_______________;G____________________;
(2)若C→D为化合反应,则此时的化学方程式_______________________________;
(3)写出E→F的化学方程式___________________________________________ ;
(4)写出反应④的离子方程式___________________________________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com