
如图所示的装置中,烧瓶中充满了干燥气体A将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。
| A(干燥气体)NO2 | b(液体) | |
| A | NO2 | 水 |
| B | CO2 | 4mol/LnaOH溶液 |
| C | Cl2 | 饱和NaCl溶液 |
| D | NH3 | 1mol/L盐酸 |
(1)选项_____________(填A、B、C、D)为何不满足要求_____________.
(2)能形成图示喷泉实验的气体和液体甚多,它们需满足的条件是①____________;②____________________。
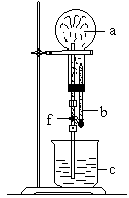
例如________气体和________液体。
(1)A、C;前者与水反应后生成NO,溶液不能充满整个烧瓶.后者气体不溶于液体.(2)①气体易溶于液体②气体与液体反应(无新气体产生);Cl2和NaOH溶液。
形成喷泉最根本的原因是瓶内外存在压强差。当烧瓶内气体溶于液体并与之反应时,瓶内气体大量减少,压强降低,外界的大气压将液体压入烧瓶内。如此持续,最后液体将充满烧瓶。B和D正确.NO2气体虽也易溶于水,但同时产生NO气体:3NO2+H2O =2HNO3+NO,即使会出现“喷泉”现象,但烧杯内的水只会部分进入烧瓶内,不会几乎充满烧瓶。
饱和氯化钠溶液不能吸收氯气,所以选项A和C错误。
从以上分析我们可知;当气体极易溶于液体或气体与液体反应(一般无新气体产生)即可形成“喷泉”,例如:Cl2和NaOH溶液等。


科目:高中化学 来源: 题型:阅读理解
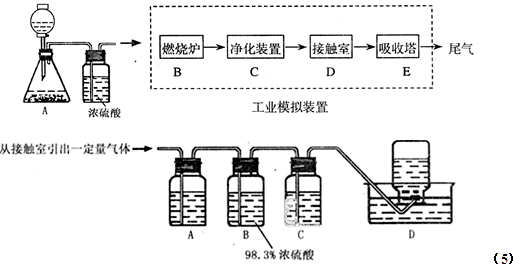
| ||
| ||
| ||
| ||
| 压强/Mpa 转化率 温度/℃ |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
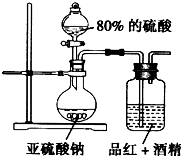 某研究性学习小组的同学决定通过实验探究SO2的漂白性是SO2本身具有的还是SO2与水作用的产物具有的,他们查阅资料知品红能溶解在酒精中形成红色溶液.
某研究性学习小组的同学决定通过实验探究SO2的漂白性是SO2本身具有的还是SO2与水作用的产物具有的,他们查阅资料知品红能溶解在酒精中形成红色溶液.- 3 |
2- 3 |
- 3 |
2- 3 |
查看答案和解析>>
科目:高中化学 来源:江苏省扬州市安宜高中2010-2011学年高二上学期期末考试化学试题(选修) 题型:058
50 ml 1.0 mol·L-1盐酸与50 mL 1.1 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量计算中和热.回答下列问题:
①从实验装置上看,大烧杯上没有________,会导致求得的中和热数值________(填“偏大”“偏小”或“无影响”);实验装置中也缺少环形玻璃搅拌棒,若用环形铜质搅拌棒代替,会导致求得的中和热数值________(填“偏大”“偏小”或“无影响”).
②若实验中分多次把NaOH溶液倒入盛有盐酸的小烧杯中,则求得的中和热数值
(填“偏大”“偏小”或“无影响”)
③若实验中改用60 mL 1.0 mol·L-1盐酸跟50 mL 1.1 mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),所求中和热________(填“相等”或“不相等”),该实验中NaOH溶液的浓度大于盐酸浓度的作用是________.
④若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会________(填“偏大”“偏小”或“无影响”).
⑤当室温低于10℃时进行实验,对实验结果会造成较大误差,其原因是________.
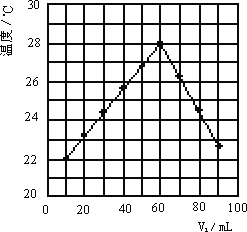
⑥若将V2 mL未知浓度的NaOH溶液,加入内盛有V1 mL 1.0 mol/L HCl溶液的小烧杯中混合均匀后测量并记录溶液温度,且每次实验中均保持V1+V2=10.0 mL,实验结果如图所示(以温度为纵坐标,V1为横坐标).做该实验时环境温度________22℃(填<、=、>),NaOH溶液的浓度约为________mol/L.
查看答案和解析>>
科目:高中化学 来源:江苏省盐城中学2011-2012学年高二上学期期中考试化学试题(选修) 题型:058
50 mL 1.0 mol·L-1盐酸与50 mL 1.1 mol·L-1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量计算中和热.回答下列问题:
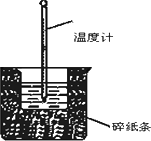
(1)从实验装置上看,大烧杯上没有________,会导致求得的中和热数值________(填“偏大”“偏小”或“无影响”);实验装置中还缺少环形玻璃搅拌棒,也会导致求得的中和热数值________(填“偏大”“偏小”或“无影响”);其中环形玻璃搅拌棒的作用为________.
(2)若实验中分多次把NaOH溶液倒入盛有盐酸的小烧杯中,则求得的中和热数值________(填“偏大”“偏小”或“无影响”).
(3)若实验中改用60 mL 1.0 mol·L-1盐酸跟60 mL 1.1 mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),所求中和热________(填“相等”或“不相等”).
(4)若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会________(填“偏大”“偏小”或“无影响”).
(5)若将V2 mL未知浓度的NaOH溶液加入盛有V1 mL 1.0 mol/L HCl溶液的小烧杯中,混合均匀后测量并记录溶液温度,且每次实验中均保持V1+V2=100 mL,实验结果如图所示(以温度为纵坐标,V1为横坐标).做该实验时起始环境温度________22℃(填<、=、>),NaOH溶液的浓度约为________mol/L.

查看答案和解析>>
科目:高中化学 来源:2012-2013学年甘肃省高三上学期期中考试化学试卷(解析版) 题型:实验题
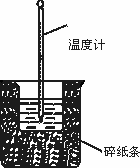
(13分)中和热的测定是高中重要的定量实验。取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:
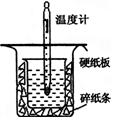
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是_________ _,除此之外,装置中的一个明显错误是 。
(2)为保证该实验成功该同学采取了许多措施,如图的碎纸条的作用在于________ ___。
(3)若改用60mL 0.25mol·L-1 H2SO4和50mL 0.55mol·L-1 NaOH溶液进行反应与上述实验相比,所放出的热量 (填“相等”、“不相等”),若实验操作均正确,则所求中和热 填“相等”“不相等”)
(4)倒入NaOH溶液的正确操作是:________。 (从下列选出)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(5)使硫酸与NaOH溶液混合均匀的正确操作是:________。 (从下列选出)。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃棒轻轻地搅动
(6)实验数据如下表:
①请填写下表中的空白:
|
温度 实验次数 |
起始温度t1℃ |
终止温度t2/℃ |
温度差平均值 (t2-t1)/℃ |
||
|
H2SO4 |
NaOH |
平均值 |
|||
|
1 |
26.2 |
26.0 |
26.1 |
29.5 |
|
|
2 |
27.0 |
27.4 |
27.2 |
32.3 |
|
|
3 |
25.9 |
25.9 |
25.9 |
29.2 |
|
|
4 |
26.4 |
26.2 |
26.3 |
29.8 |
②近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热ΔH=______ ____ ( 取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)____ ____。
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com