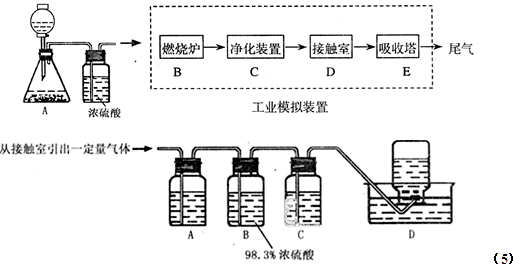
某化学兴趣小组的同学为模拟工业制造硫酸的生产过程,设计了如图所示的装置,请根据图回答问题:
(1)装置A用来制取氧气,写出相应的化学方程式
2H
2O
22H
2O+O
2↑或2Na
2O
2+2H
2O=4NaOH+O
2↑
2H
2O
22H
2O+O
2↑或2Na
2O
2+2H
2O=4NaOH+O
2↑
;
(2)燃烧炉内放一定量黄铁矿粉末,在高温条件下和A装置制出的氧气充分反应,其化学方程式为
;现有含FeS
260%的黄铁矿100t,如果在煅烧的过程中,S损失了18%,则可生产质量分数为98%的硫酸
82t
82t
吨.
(3)C装置为净化装置,若无该装置,将混合气体直接通入D装置,除对设备有腐蚀外,还会造成的后果是
催化剂中毒
催化剂中毒
;
(4)工业上利用2SO
2(g)+O
2(g)═2SO
3(g)反应制备SO
3,下表是在一定条件下测定的SO
2的转化率,根据表格中提供的数据,请选择工业利用该反应制备SO
3的温度与压强
常压、400℃~500℃
常压、400℃~500℃
.
压强/Mpa
转化率
温度/℃ |
0.1 |
0.5 |
1 |
10 |
| 400 |
99.2 |
99.6 |
99.7 |
99.9 |
| 500 |
93.5 |
96.9 |
97.8 |
99.3 |
| 600 |
73.7 |
85.8 |
89.5 |
96.4 |
(5)为检验从接触室出来的气体成分,甲同学设计如下实验:
①A中盛放的试剂是
BaCl2溶液
BaCl2溶液
;
②B中盛放98.3%浓硫酸的作用是
除SO3气体
除SO3气体
,乙同学提出可用饱和NaHSO
3溶液代替98.3%的浓硫酸,请你判断乙同学的方案
不可行
不可行
(填“可行”或“不可行”),说明理由
SO3与NaHSO3反应生成SO2,对实验结果造成干扰
SO3与NaHSO3反应生成SO2,对实验结果造成干扰
;
③C中盛放的试剂是
酸性KMnO4溶液或溴水
酸性KMnO4溶液或溴水
,其作用是
检验并吸收SO2
检验并吸收SO2
;
(6)在硫酸工业的尾气中,SO
2是主要大气污染物,必须进行净化处理,处理方法可采用过量氨气吸收,反应的离子方程式是
SO2+2NH3?H2O=SO32-+2NH4+
SO2+2NH3?H2O=SO32-+2NH4+
.





