
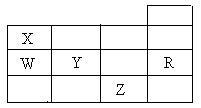
| A.通常情况下五种元素的单质中,Z单质的沸点最高 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.W的氢化物的沸点比X的氢化物的沸点高 |
| D.元素最高价氧化物对应的水化物的酸性Y比W强 |
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氧化性强弱:F2<Cl2 | B.金属性强弱:K<Na |
| C.酸性强弱:H3PO4<H2SO4 | D.碱性强弱:NaOH<Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:Y>Z>R>T |
| B.气态氢化物的稳定性:W<R<T |
| C.最高价氧化物对应的水化物碱性:X>Z |
| D.XR2、WR2两化合物含有的化学键的类型相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
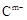 、
、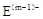 具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题: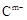 、
、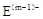 的还原性强弱顺序为:_________,(用离子符号表示)能证明其还原性强弱的离子方程式为________________________________。
的还原性强弱顺序为:_________,(用离子符号表示)能证明其还原性强弱的离子方程式为________________________________。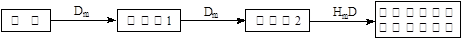
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
族 周期 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | ⑦ | | ⑨ | ⑧ | |
 (2)②⑦⑨的最高价含氧酸的酸性由强到弱的顺序为________________________。
(2)②⑦⑨的最高价含氧酸的酸性由强到弱的顺序为________________________。 (3)①、④、⑤中的某些元素可形成既含离子键又含共价键的化合物,写出其中两种化合物的电子式: ___、 。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的化合物,写出其中两种化合物的电子式: ___、 。 (4)元素④的一种氢化物A在一定条件下分解为它的另一种氢化物B,写出A的结构式_______
(4)元素④的一种氢化物A在一定条件下分解为它的另一种氢化物B,写出A的结构式_______ 。
。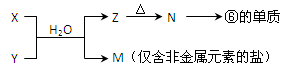
 X溶液与Y溶液反应的离子方程式为_____________________
X溶液与Y溶液反应的离子方程式为_____________________  N→⑥的单质的化学方程式为_____________ _
N→⑥的单质的化学方程式为_____________ _ 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径D <C <B<A | B.原子序数 d > c > a > b |
| C.离子半径C>D>B> A | D.单质的氧化性C > D > A >B |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com