
【题目】NA为阿伏伽德罗常数,下列说法正确的是( )
A.1molC2H6中含有6 NA个共价键
B.7.8 g Na2O2中含有的阳离子数和阴离子数均为0.2NA
C.14.0g由C2H4和C3H6组成的混合气体原子总数为3NA
D.5.6g金属铁与足量盐酸反应时失去的电子数是0.3NA
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某实验小组依据反应AsO43﹣+2H++2I﹣AsO33﹣+I2+H2O设计如图1,电池,探究pH对AsO43﹣氧化性的影响,测得输出电压与pH的关系如图2.下列有关叙述错误的是( ) 
A.c点时,正极的电极反应为ASO43﹣+2H++2e﹣═AsO33﹣+H2O
B.b点时,反应处于化学平衡状态
C.a点时,盐桥中K+向左移动
D.pH>0.68时,氧化性I2>AsO43﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物的结构简式为 ![]()
(1)该有机物中所含官能团的名称是 .
(2)该有机物发生加成聚合反应后,所得产物的结构简式为 .
(3)写出该有机物发生消去反应的化学方程式(注明反应条件): .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:
物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
请回答下列问题:
(1)试管A内在60~80℃时发生的主要反应的化学方程式为(注明反应条件);
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在;目的是;当试管A内的主要反应完成后温度计水银球的位置应在 , 目的是;
(3)烧杯B的作用是;烧杯B内盛装的液体可以是(写出一种即可,在题给物质中找);
(4)若想检验试管C中是否含有产物乙酸,请你在所提供的药品中进行选择,设计一个简便的实验方案.所提供的药品有:pH试纸、红色的石蕊试纸、白色的醋酸铅试纸、碳酸氢钠粉末.实验仪器任选.该方案为:
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应中反应物与生成物有:FeCl2、FeCl3、CuCl2、Cu. 
(1)将上述反应设计成的原电池如图甲所示,请回答下列问题: ①图中X溶液是;②Cu电极上发生的电极反应式为;
③原电池工作时,盐桥中的离子(填“K+”或“Cl﹣”)不断进入X溶液中.
(2)将上述反应设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题: ①M是极;②图丙中的②线是离子的变化.
③当电子转移为2mol时,向乙烧杯中加入L 5molL﹣1NaOH溶液才能使所有的金属阳离子沉淀完全.
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点. ①高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O ![]() Na2FeO4+3H2↑,则电解时阳极的电极反应式是 .
Na2FeO4+3H2↑,则电解时阳极的电极反应式是 .
②高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为 .
③Na2FeO4能消毒、净水的原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( ) ①Al2O3 ![]() NaAlO2(aq)
NaAlO2(aq) ![]() Al(OH)3
Al(OH)3
②S ![]() SO3
SO3 ![]() H2SO4
H2SO4
③饱和NaCl(aq) ![]() NaHCO3
NaHCO3 ![]() Na2CO3
Na2CO3
④Fe2O3 ![]() FeCl3(aq)
FeCl3(aq) ![]() 无水FeCl3
无水FeCl3
⑤MgCl2(aq) ![]() Mg(OH)2
Mg(OH)2 ![]() MgO.
MgO.
A.①③⑤
B.②③④
C.②④⑤
D.①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤炭可以转化为清洁能源和化工原料.
(1)用煤可以制得水煤气.工业上可用煤和水通过水煤气法制氢气,已知下列热化学方程式:
C(s)+ ![]() O2(g)═CO(g)△H1=﹣110.5kJmol﹣1
O2(g)═CO(g)△H1=﹣110.5kJmol﹣1
2H2(g)+O2(g)═2H2O(g)△H2=﹣483.6kJmol﹣1
试求水煤气法制氢气的反应的反应热△H3 .
C(s)+H2O(g)═CO(g)+H2(g)△H3=kJmol﹣1
(2)若H﹣H、O=O和O﹣H键的键能分别是436kJmol﹣1、496kJmol﹣1和m kJmol﹣1 , 结合上述热化学方程式的相关数据计算,m= .
(3)已知一氧化碳与水蒸气反应过程的能量变化如图所示:则此反应为(填“吸热”或“放热”)反应,反应的热化学方程式为 . 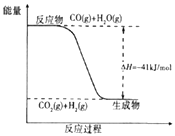
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com