
分析 发生反应:Fe+H2SO4=FeSO4+H2↑,根据n=$\frac{m}{M}$计算Fe的物质的量,根据方程式计算生成氢气、参加反应H2SO4的物质的量,根据V=nVm计算生成氢气体积,根据V=$\frac{n}{c}$计算消耗硫酸的体积.
解答 解:Fe的物质的量为$\frac{11.2g}{56g/mol}$=0.2mol,则:
Fe+H2SO4=FeSO4+H2↑
0.2mol 0.2mol 0.2mol
故标况下生成氢气体积为0.2mol×22.4L/mol=4.48L,
消耗硫酸的体积为$\frac{0.2mol}{0.2mol/L}$=1L,
答:标况下生成氢气体积为4.48L,消耗硫酸的体积为1L.
点评 本题考查物质的量的有关计算,比较基础,旨在考查学生对基础知识的理解掌握.


科目:高中化学 来源: 题型:解答题
 某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如右表所示.
某学习小组依据反应:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0,设计制备磺酰氯(SO2Cl2)的装置如图,有关信息如右表所示.| SO2Cl2 | Cl2 | SO2 | |
| 熔点/℃ | -54.1 | -101 | -72.4 |
| 沸点/℃ | 69.1 | -34.6 | -10 |
| 性质 | 遇水发生 剧烈水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制作宇航员航天服的聚酯纤维不属于新型无机非金属材料 | |
| B. | 煤的主要成分为单质碳、苯、二甲苯等,可通过煤的干馏将它们分离 | |
| C. | PM2.5是指粒径在2.5微米以下的颗粒物,其在空气中形成的分散系属于胶体 | |
| D. | 为防止中秋月饼等富脂食品氧化变质,常在包装中放入生石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

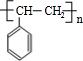
 ,⑥
,⑥ .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只能是1:1 | B. | 只能是3:1 | C. | 只能是4:1 | D. | 任意比 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H2 C2H6 | B. | CH4 C3H8 | C. | C3H6 C3H8 | D. | C2H4 C4H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com