
【题目】化学反应H2(g) + I2(g) ![]() 2HI(g)在持续加热的条件下,向密闭容器中充入2 mol H2和3 mol I2(g),充分反应后,该密闭容器中
2HI(g)在持续加热的条件下,向密闭容器中充入2 mol H2和3 mol I2(g),充分反应后,该密闭容器中
A. 2 mol H2已耗尽 B. 3 mol I2(g)已耗尽
C. HI的物质的量等于4 mol D. HI的物质的量少于4 mol
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】己知:|||+ ![]()
![]()
![]() ,如果要合成
,如果要合成 ![]() ,所用的起始原料可以是( ) ①2﹣甲基﹣1,3﹣丁二烯和2﹣丁炔
,所用的起始原料可以是( ) ①2﹣甲基﹣1,3﹣丁二烯和2﹣丁炔
②1,3﹣戊二烯和2﹣丁炔
③2,3﹣二甲基﹣1,3﹣戊二烯和乙炔
④2,3﹣二甲基﹣1,3﹣丁二烯和丙炔.
A.①④
B.②③
C.①③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2和N2O4可以相互转化:2NO2(g)N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法错误的是( ) 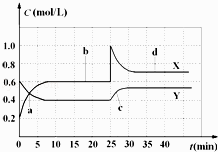
A.图中共有两条曲线X和Y,其中曲线X表示NO2浓度随时间的变化
B.a、b、c、d四个点中,表示化学反应处于平衡状态的点是b和d
C.反应进行至25min时,曲线发生变化的原因是加入0.4mol N2O4
D.若要达到与d相同的状态,在25min时还可以采取的措施是适当缩小容器体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇被称为21世纪的新型燃料,工业上通过下列反应①和②,用CH4和H2O为原料来制备甲醇. ①CH4(g)+H2O(g)CO(g)+3H2(g)△H1
②CO(g)+2H2(g)CH3OH(g)△H2
将0.20mol CH4(g)和0.30mol H2O(g)通入容积为10L的密闭容器中,在一定条件下发生反应①,达到平衡时,CH4的转化率与温度、压强的关系如图.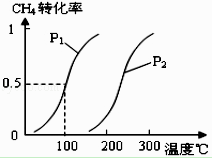
(1)温度不变,缩小体积,增大压强,①的反应速率(填“增大”、“减小”或“不变”),平衡向方向移动.
(2)温度升高,反应①的△H10(填“<”、“=”或“>”),其平衡常数表达式为K= , 100℃时的平衡常数值是 .
(3)在压强为0.1MPa条件下,将a mol CO与 3a mol H2的混合气体在催化剂作用下进行反应②生成甲醇.为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中.请在下表空格中填入剩余的实验条件数据.
实验编号 | T(℃) | n (CO)/n(H2) | P(MPa) |
I | 150 | 1/3 | 0.1 |
II | 5 | ||
III | 350 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某个容积为2L的密闭容器内,在T℃时按图1所示发生反应: 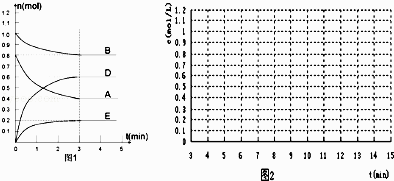
mA(g)+nB(g)pD(g)+qE(s)H<0(m、n、p、q为最简比例的整数).
(1)根据图1所示,反应开始至达到平衡时,用D表示该反应速率为mol/(Lmin); 方程式中m:n:p:q=
(2)该反应的化学平衡常数K为(保留至一位小数);
(3)下列措施能增大B的转化率的是 A.升高温度 B.保持体积不变通入1molB
C.保持体积不变移出部分物质D(g) D.将容器的容积增大为原来的2倍
E.保持体积不变通入1mol A
(4)能判断该反应已经达到化学平衡状态的是 A.恒容恒温时容器中气体压强保持不变 B.混合气体中D浓度不变
C.v(A)正=v(A)逆 D.恒容时容器中气体密度不变
(5)反应达到平衡后,第7min时,改变条件,在第9min达到新的平衡,在图2上作出第7min至第15min 下列情况下,D浓度变化图像
①若降低温度且平衡时D物质的量变化了0.4mol (用虚线)
②若将容器的容积压缩为原来一半(用实线)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下图A、B、C三个装置,回答下列问题:
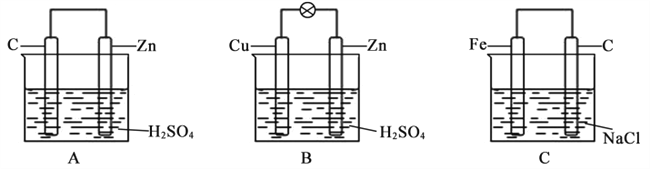
(1)把一块纯净的锌片插入装有稀硫酸的烧杯中,可观察到锌片上有气泡,再平行插入一碳棒,可观察到碳棒上______(填“有”或“没有”)气泡产生。用导线把锌片和碳棒连接起来组成一个原电池(图A),正极的反应式为______________。
(2)如果烧杯中最初装入的是500 mL2 mol/L硫酸溶液,构成铜锌原电池(图B,假设产生的气体没有损失),当收集到11.2 L(标准状况下)H2时,溶液体积变化忽略不计,则烧杯内溶液中溶质及其物质的量浓度为________。
(3)如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(图C),放置数天后,铁片生锈。负极反应式为___________。
(4)将铜粉末用10% H2O2和3.0 mol/L的H2SO4混合溶液处埋,测得不同温度下铜的平均溶解速率如下表:
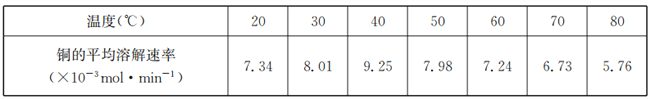
由表中数据可知,当温度高于40℃时,铜的平均溶解速率随着温度的升高而下降,其主要原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g)![]() 4C(g)+2D(g),在不同条件下反应,其平均反应速率v(X)如下,其中反应速率最快的是
4C(g)+2D(g),在不同条件下反应,其平均反应速率v(X)如下,其中反应速率最快的是
A. v(C)=0.2mol(L·s) B. v(D)=6mol (L·min)
C. V(A)=4mol(L·min) D. v(B)=8mol(L·min)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com