
【题目】观察下图A、B、C三个装置,回答下列问题:
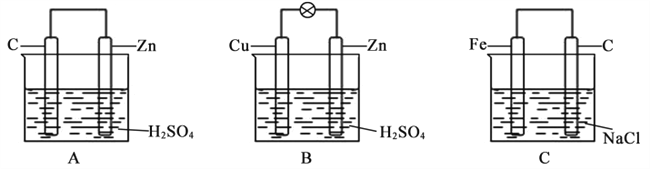
(1)把一块纯净的锌片插入装有稀硫酸的烧杯中,可观察到锌片上有气泡,再平行插入一碳棒,可观察到碳棒上______(填“有”或“没有”)气泡产生。用导线把锌片和碳棒连接起来组成一个原电池(图A),正极的反应式为______________。
(2)如果烧杯中最初装入的是500 mL2 mol/L硫酸溶液,构成铜锌原电池(图B,假设产生的气体没有损失),当收集到11.2 L(标准状况下)H2时,溶液体积变化忽略不计,则烧杯内溶液中溶质及其物质的量浓度为________。
(3)如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(图C),放置数天后,铁片生锈。负极反应式为___________。
(4)将铜粉末用10% H2O2和3.0 mol/L的H2SO4混合溶液处埋,测得不同温度下铜的平均溶解速率如下表:
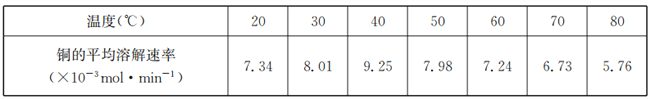
由表中数据可知,当温度高于40℃时,铜的平均溶解速率随着温度的升高而下降,其主要原因是________________。
【答案】 没有 2H++2e-=H2↑ c(H2SO4)=1mol/L c(ZnSO4)=1mol/L Fe-2e-=Fe2+ 温度越高,H2O2越容易分解(或其他合理答案)
【解析】(1)把一块纯净的锌片插入装有稀硫酸的烧杯中,锌与稀硫酸反应生成氢气,可观察到锌片上有气泡,再平行插入一碳棒,碳与稀硫酸不反应,因此碳棒上没有气泡产生;锌片、碳棒和硫酸形成的原电池中,碳棒为正极,该极上氢离子得电子生成氢气,电极反应为: 2H++2e-=H2↑;正确答案:没有;2H++2e-=H2↑。
(2) 根据正极反应: 2H++2e-=H2↑,当在标准状况下收集到11.2L即0.5mol的氢气时,转移电子是1mol,减少的氢离子为1mol,所以剩余的硫酸的量为0.5 mol,其浓度为0.5/0.5=1mol/L;负极上的电极反应式为:Zn-2e-=Zn,当转移电子1mol时,生成锌离子的量为0.5mol,所以c(ZnSO4)=0.5/0.5=1mol/L ;正确答案:c(H2SO4)=1mol/L;c(ZnSO4)=1mol/L。
(3) 铁片、石墨和氯化钠溶液构成的原电池中,金属铁发生吸氧腐蚀,正极上是氧气得电子发生还原反应,负极是铁失电子变为亚铁离子,发生氧化反应,电极反应为:Fe-2e-=Fe2+;正确答案:Fe-2e-=Fe2+。
(4)双氧水具有强氧化性和不稳定性,温度太高,双氧水易发生分解,氧化能力降低,铜的平均溶解速率随着温度的升高而下降,因此要控制反应的温度不能过高;正确答案:温度越高,H2O2越容易分解(或其他合理答案)。


科目:高中化学 来源: 题型:
【题目】化学反应H2(g) + I2(g) ![]() 2HI(g)在持续加热的条件下,向密闭容器中充入2 mol H2和3 mol I2(g),充分反应后,该密闭容器中
2HI(g)在持续加热的条件下,向密闭容器中充入2 mol H2和3 mol I2(g),充分反应后,该密闭容器中
A. 2 mol H2已耗尽 B. 3 mol I2(g)已耗尽
C. HI的物质的量等于4 mol D. HI的物质的量少于4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.水的电离是吸热过程,升高温度,水的离子积增大、pH减小
B.用金属活动性顺序可解释反应:Na(l)+KCl(l)═NaCl(l)+K(g)
C.对于平衡2HI(g)I2(g)+H2(g),压缩容器体积,平衡不移动,气体的颜色不变
D.由反应SiO2+2C ![]() Si+2CO↑,可得出C的非金属性强于Si
Si+2CO↑,可得出C的非金属性强于Si
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)某密闭容器中发生反应:X(g)+Y(g)3Z(g)△H<0如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( ) 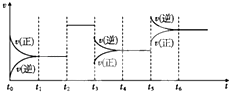
A.t2时加入了催化剂
B.t3时降低了温度
C.t5时增大了压强
D.t4~t5时间内转化率最低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A. 标准状况下,1LHCl和1LH2O的物质的量相同
B. 标准状况下,1gH2和14gN2的体积相同
C. 28gCO的体积为22.4L
D. 两种物质的物质的量相同,则它们在标准状况下的体积也相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A只含有C、H、O三种元素,且它们的质量比为9:2:4;A的核磁共振氢谱显示有四种不同类型的氢原子.物质D是一种芳香族化合物,请根据如图(所有无机产物已略去)中各有机物的转化关系回答问题. RCHO+R′CH2CHO ![]()
![]() +H2O
+H2O
已知,两分子醛在一定条件下可以发生如下反应(其中R、R′为H或烃基):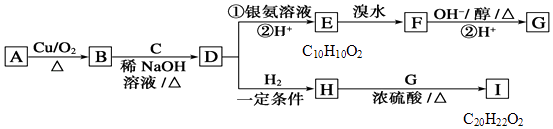
(1)写出质A的名称:;C的结构简式:;E中含氧官能团的名称: .
(2)写出下列反应的有机反应类型:A→B; D→H .
(3)写出H到I的化学方程式: .
(4)写出D到E过程中的①的反应化学方程式: .
(5)1molF与足量的氢氧化钠水溶液反应最多消耗mol NaOH.
(6)根据题中信息,G的可能结构为种.
(7)请写出符合下列条件的E的同分异构体的结构简式 . i.该物质水解产物之一为乙酸; ii.苯环上的一氯代物只有两种结构.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】席夫碱类化合物G在催化、药物、新材料等方面有广泛应用.合成G的一种路线如下: 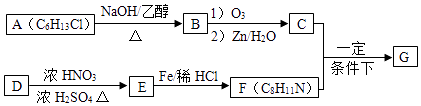
已知以下信息:
① 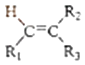
![]() R1CHO+
R1CHO+ 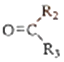
②1mol B经上述反应可生成2mol C,且C不能发生银镜反应
③D属于单取代芳烃,其相对分子质量为106
④核磁共振氢谱显示F苯环上有两种化学环境的氢原子
⑤RNH2+ 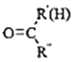
![]()
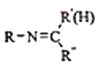 +H2O
+H2O
回答下列问题:
(1)C中官能团名称 , D的化学名称 .
(2)由A生成B的化学方程式为 .
(3)G的结构简式为 .
(4)F的同分异构体中含有苯环的还有种(不考虑立体异构),其中核磁共振氢谱有4组峰,且面积比为6:2:2:1的是(写出其中一种的结构简式).
(5)由苯及化合物C经如下步骤可合成N﹣异丙基苯胺: ![]()
![]() H
H ![]() I
I ![]() J
J ![]()
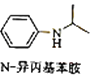
反应条件1所选择的试剂为 , H→I的反应类型为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com