
【题目】下列说法中不正确的是( )
A.浓度均为0.1 molL-1的小苏打溶液与烧碱溶液等体积混合:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-)
B.pH相同的盐酸和硫酸,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液pH相等,则m>n
C.常温下,0.1 molL-1某一元酸HA在水中有0.1%发生电离,则该温度下HA的电离常数约为10-7
D.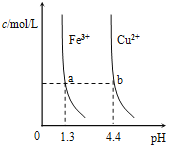 某温度下,Fe(OH)3,Cu(OH)2分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度的变化如图。由图可知:Ksp[Fe(OH)3]<Ksp[Cu(OH)2]
某温度下,Fe(OH)3,Cu(OH)2分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度的变化如图。由图可知:Ksp[Fe(OH)3]<Ksp[Cu(OH)2]
【答案】B
【解析】
A.浓度相等体积相等的小苏打溶液与烧碱溶液混合,二者恰好反应产生Na2CO3,根据电荷守恒可知:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-),A正确;
B.盐酸、硫酸都是强酸,完全电离,pH相同的盐酸和硫酸,溶液中c(H+)相等,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液pH相等,说明稀释后溶液中c(H+)仍然相等,因此稀释倍数m=n,B错误;
C. HA是一元弱酸,在溶液中存在电离平衡,由HA![]() H++A-,在常温下,0.1 molL-1某一元酸HA在水中有0.1%发生电离,则c(H+)=c(A-)=0.1 mol/L×0.1%=10-4 mol/L,c(HA)=0.1 mol/L-10-4 mol/L≈0.1 mol/L,所以该弱酸在常温下的电离平衡常数为K=
H++A-,在常温下,0.1 molL-1某一元酸HA在水中有0.1%发生电离,则c(H+)=c(A-)=0.1 mol/L×0.1%=10-4 mol/L,c(HA)=0.1 mol/L-10-4 mol/L≈0.1 mol/L,所以该弱酸在常温下的电离平衡常数为K=![]() =1×10-7,C正确;
=1×10-7,C正确;
D.Ksp[Fe(OH)3]=c(Fe3+)·c3(OH-)= c(Fe3+)· (10-12.7) 3;Ksp[Cu(OH)2]= c(Cu2+)·c2(OH-)= c(Cu2+)· (10-9.6)2;由于c(Fe3+)=c(Cu2+),所以Ksp[Fe(OH)3]< Ksp[Cu(OH)2],D正确;
故合理选项是B。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】SO2的含量是空气质量日报中一项重要检测指标,也是最近雾霾天气肆虐我国大部分地区的主要原因之一。加大SO2的处理力度,是治理环境污染的当务之急。
I.电化学法处理SO2。
硫酸工业尾气中的SO2经分离后,可用于制备硫酸,同时获得电能,装置如右图所示(电极均为惰性材料):

(1)M极发生的电极反应式为________________。
(2)若使该装置的电流强度达到2.0A,理论上每分钟应向负极通入标准状况下气体的体积为________L(已知:1个e-所带电量为1.6×10-19C)。
Ⅱ.溶液与电化学综合(钠碱循环法)处理SO2。
(3)钠碱循环法中,用Na2SO3溶液作为吸收液来吸收SO2,该反应的离子方程式为______________。
(4)吸收液吸收SO2的过程中,pH随n(SO32-)/n(HSO3-)变化关系如右图所示:
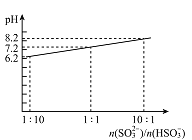
①用图中数据和变化规律说明NaHSO3溶液呈酸性的原因________________。
②n(SO32-)/n(HSO3-)=1:1时,溶液中离子浓度由大到小的顺序是_____________。
(5)当吸收液的pH降至约为6时,需送至电解槽处理,直至得到pH>8的吸收液再循环利用,其电解示意图如下:
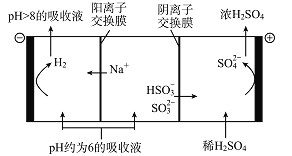
①写出阳极发生的电极反应式________________;
②当电极上有2 mol电子转移时阴极产物的质量为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在漂白液(次氯酸钠溶液)中:Ag+、K+、NO3-、SO32-
B.中性溶液:K+、NO3-、Br-、Fe3+
C.![]() =1012的溶液中,NH4+、Ca2+、Cl-、NO3-
=1012的溶液中,NH4+、Ca2+、Cl-、NO3-
D.由水电离的c(H+)=1×10-10mol/L的溶液中:K+、Na+、HCO3-、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭容器中通入一定量的A、B,发生反应A(g)+2B(g)![]() 3C(g)。如图是A的反应速率v(A)随时间变化的示意图。下列说法正确的是( )
3C(g)。如图是A的反应速率v(A)随时间变化的示意图。下列说法正确的是( )

A.反应物A的浓度:a点小于b点
B.该反应的某种生成物可能对反应起催化作用
C.曲线上的c、d两点都表示达到平衡状态
D.A的平均反应速率:ab段大于bc段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1 mol/L CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起( )
A. 溶液的pH增大
B. CH3COOH电离度增大
C. 溶液的导电能力减弱
D. 溶液中c(OH-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见图。下列叙述正确的是( )
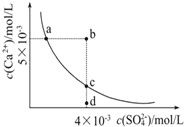
①a、c两点均可以表示CaSO4溶于水所形成的饱和溶液
②a点对应的Ksp不等于c点对应的Ksp
③b点对应的溶液将有沉淀生成
④d点溶液通过蒸发溶剂可以变到c点
⑤常温下CaSO4溶于水的饱和溶液中,c(Ca2+)与c(SO42-)的乘积对应曲线上任意一点
⑥常温下,向100 mL饱和CaSO4溶液中加入400 mL0.01 mol/L Na2SO4溶液,能使溶液由a点变为b点
A.2句B.3句C.4句D.5句
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向10mL一定浓度的HCOOH溶液中不断滴加1mol·L-1的NaOH溶液,并一直保持常温,所加碱的体积与-lgc水(H+)的关系如图所示。c水(H+)为溶液中水电离的c(H+)。下列说法不正确的是( )

A.常温下,Ka(HCOOH)的数量级为10-4
B.a、b两点的pH均为7
C.从a点到b点,水的电离程度先增大后减小
D.混合溶液的导电性逐渐增强
查看答案和解析>>
科目:高中化学 来源: 题型:
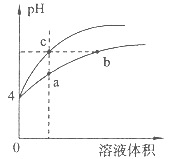
【题目】某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是
A. a、c两点溶液的导电能力相同
B. b点溶液中c(H+)+c(NH3·H2O)=c(OH-)
C. a、b、c三点溶液中水的电离程度a>b>c
D. 用等浓度NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液体积Vb=Vc
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知Ksp(AgCl)=1.8×10-10,则将AgCl放在蒸馏水中形成饱和溶液,溶液中的c(Ag+)是________?
(2)已知Ksp[Mg(OH)2]=1.8×10-11,则将Mg(OH)2放入蒸馏水中形成饱和溶液,溶液的pH为________?
(3)在0.01 mol·L-1的MgCl2溶液中,逐滴加入NaOH溶液,刚好出现沉淀时,溶液的pH是________?当Mg2+完全沉淀时,溶液的pH为________?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com