
【题目】将0.1 mol/L CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起( )
A. 溶液的pH增大
B. CH3COOH电离度增大
C. 溶液的导电能力减弱
D. 溶液中c(OH-)减小
【答案】A
【解析】
试题A.CH3COOH溶液加水稀释,CH3COOH的电离平衡CH3COOH![]() CH3COO-+H+向正反应方向移动,溶液的pH增加,向CH3COOH溶液加入少量CH3COONa晶体时,溶液中c(CH3COO-)增大,醋酸的电离平衡向逆反应方向移动,溶液的pH增加,正确;B.CH3COOH溶液加水稀释,平衡向正反应方向移动,电离程度增大,加入少量CH3COONa晶体时平衡向逆反应方向移动,电离程度减小,错误;C.CH3COOH溶液加水稀释,离子浓度减小,溶液的导电能力减弱,加入少量CH3COONa晶体时,离子浓度增大,溶液的导电能力增强,错误;D.加水稀释,促进醋酸电离,但溶液中氢离子浓度减小,加入少量CH3COONa晶体时平衡向逆反应方向移动,电离程度减小,氢离子浓度减小,温度不变,水的离子积常数不变,所以氢氧根离子浓度增大,错误。
CH3COO-+H+向正反应方向移动,溶液的pH增加,向CH3COOH溶液加入少量CH3COONa晶体时,溶液中c(CH3COO-)增大,醋酸的电离平衡向逆反应方向移动,溶液的pH增加,正确;B.CH3COOH溶液加水稀释,平衡向正反应方向移动,电离程度增大,加入少量CH3COONa晶体时平衡向逆反应方向移动,电离程度减小,错误;C.CH3COOH溶液加水稀释,离子浓度减小,溶液的导电能力减弱,加入少量CH3COONa晶体时,离子浓度增大,溶液的导电能力增强,错误;D.加水稀释,促进醋酸电离,但溶液中氢离子浓度减小,加入少量CH3COONa晶体时平衡向逆反应方向移动,电离程度减小,氢离子浓度减小,温度不变,水的离子积常数不变,所以氢氧根离子浓度增大,错误。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】25℃时,5种银盐的溶度积常数(Ksp)分别是:
AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
下列说法不正确的是
A. 氯化银、溴化银和碘化银的溶解度依次减小
B. 将硫酸银溶解于水后,向其中加入少量硫化钠固体,能得到黑色沉淀
C. 在5mL1.5×10-5mol/L的NaCl溶液中,加入1滴(1mL约20滴)1.0×10-3mol/L的AgNO3溶液,不能观察到白色沉淀
D. 在烧杯中放入6.24g硫酸银固体,加200g水,经充分溶解后,所得饱和溶液的体积为200mL,溶液中Ag+的物质的量浓度为0.2mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注,下述为制取Cu2O的两种方法:
方法a:用炭粉在高温条件下还原CuO
方法b:电解法,反应为2Cu+H2O![]() Cu2O+H2↑
Cu2O+H2↑
(1)已知:①2Cu(s)+![]() O2(g)=Cu2O(s)△H1=akJ/mol
O2(g)=Cu2O(s)△H1=akJ/mol
②C(s)+![]() O2(g)=CO(g) △H2=bkJ/mol
O2(g)=CO(g) △H2=bkJ/mol
③Cu(s)+![]() O2(g)=CuO(s)△H3=ckJ/mol
O2(g)=CuO(s)△H3=ckJ/mol
则方法a中反应的热化学方程式是:_________________。
(2)方法b是用肼燃料电池为电源,通过离子交换膜电解法控制电解液中OH-的浓度而制备纳米Cu2O装置如图所示:
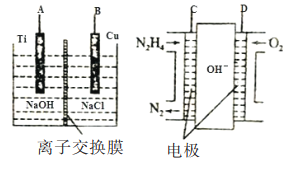
①如图装置中D电极应连______电极。(填“A”或“B”)
②该离子交换膜为______离子交换膜(填“阴”或“阳”),该电解池的B极反应式为:______。
③C极反应式为:__________。
(3)在相同体积的恒容密闭容器中,用以上方法制得的两种Cu2O分别进行催化分解水的实验:
2H2O![]() 2H2(g)+O2(g) △H>0,水蒸气的浓度随时间t变化如表所示:
2H2(g)+O2(g) △H>0,水蒸气的浓度随时间t变化如表所示:
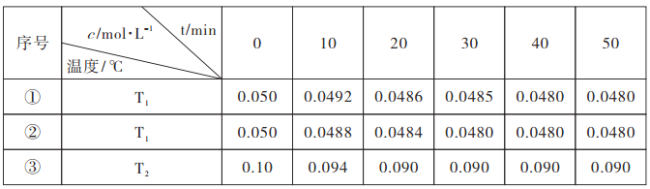
根据上述数据分析:
①催化剂的效率:实验①_______实验②(填“>”或“<”);
②通过实验①、③分析,T1______T2(填“>”或“<”);
③实验①、②、③的化学平衡常数K1、K2、K3的大小关系为:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B3C+4D中,表示该反应速率最快的是( )
A. υ(A)=0.5molL1S1 B. υ(B)=0.3 molL1S1
C. υ(C)=1.2molL1min1 D. υ(D)=0.6 molL1min1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示。已知 W 的一种核素的质量数为18,中子数为10;X 和 Ne 的核外电子数相差1; 在Z所在的周期中,Z 元素的原子得电子能力最强;四种元素的最外层电子数之和为18。 请回答下列问题:
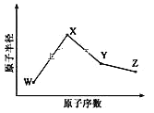
(1)X 元素位于元素周期表中位置为____________。
(2)Z 的同族简单氢化物中,稳定性最好的是________(写化学式),原因__________________。
(3)W、X、Z 三种元素形成的化合物中化学键类型为___________;X2W2的电子式为________。
(4)Y 与 Z 形成的化合物YZ4在常温下是一种液态,它和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式为__________________________。
(5)Z 的氧化物很多,其中一种黄绿色气体M,其氧含量为 47.41%,可用于水处理, M 在液态和浓缩气态时具有爆炸性。 M 可与 NaOH 溶液反应生成两种稳定的盐,它们的物质的量之比为 1︰5,该反应的化学方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫铁矿(主要成分为![]() )为原料制备氯化铁晶体(
)为原料制备氯化铁晶体(![]() )的工艺流程如下所示:
)的工艺流程如下所示:

下列说法不正确的是
A. “酸溶”过程中使用的酸也可以是硝酸
B. 为防止污染,“焙烧”过程中产生的![]() 应回收利用
应回收利用
C. 通入氯气的目的是氧化![]()
D. 用![]() 制取无水
制取无水![]() 时,需要在氯化氢气流中加热
时,需要在氯化氢气流中加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,电流表指针发生偏转,同时A极质量减少,B极上有气泡产生,C为电解质溶液,

下列说法错误的是
A. B极为原电池的正极
B. A、B、C可能分别为Zn、Cu、稀盐酸
C. C中阳离子向A极移动
D. A极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含硒(Se)的保健品已开始进入市场。已知硒与氧、硫同主族,与溴同周期,则下列关于硒的叙述中,正确的是
A.非金属性比硫强B.原子序数为34
C.氢化物比HBr稳定D.最高价氧化物的水化物显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲苯是重要的有机化工原料,以甲苯为原料,制备香料、药物中间体(M)和高分子化合物(N)的一种合成路线如下:

已知:R1CHO+R2CH2CHO![]()
![]()
![]()
![]() (R1、R2表示氢原子或烃基)。
(R1、R2表示氢原子或烃基)。
请回答下列问题:
(1)B中官能团的名称为______________________,E的化学名称为____________________。
(2)H→N的反应类型为_______________________________。
(3)G分子中最多有________个碳原子共平面。顺式-N的结构简式为_____________________。
(4)C+D→M的化学方程式为_________________________________________。
(5)同时满足下列条件的H 的同分异构体有___________种(不考虑立体异构)。
①苯环上连接2个取代基
②能发生银镜反应,且1mol最多生成4molAg
(6)参照上述合成路线和信息,写出以甲醇和乙醛为原料(无机试剂任选),设计制备![]() 的合成路线:______________________________________________。
的合成路线:______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com