
【题目】某课外活动小组用如图所示装置进行实验,请回答下列问题:
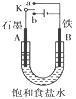
(1)若开始实验时开关K与a连接,则B极的电极反应式为_________。
(2)若开始实验时开关K与b连接,则下列说法正确的是_____(填序号)。
①溶液中Na+向A极移动
②从A极逸出的气体能使湿润的淀粉KI试纸变蓝
③反应一段时间后向电解液中加适量盐酸可使其恢复到电解前的浓度
(3)该小组运用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。
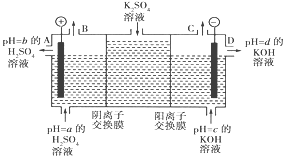
①该电解槽的阳极反应式为_________,通过阴离子交换膜的离子数____(填“>”“<”或“=”)通过阳离子交换膜的离子数;
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为____;
③电解一段时间后,B口与C口产生气体的质量比为___。
【答案】Fe-2e-=Fe2+ ② 2H2O-4e-=O2↑+4H+(写4OH--4e-=2H2O+O2↑也可) < b<a<c<d 8∶1
【解析】
(1)开关与a点相连接时形成的是原电池,铁为原电池的负极,失去电子;
(2)当开关与b点连接时,形成的装置是电解池,石墨与电源的正极相连为阳极,铁与电源的负极相连,为阴极,据此判断;
(3)①电解硫酸钾溶液,阳极发生氧化反应,OH-被氧化生成O2,SO42-通过阴离子交换膜向阳极移动,钾离子通过阳离子交换膜向阴极移动;
②OH-被氧化,阳极生成H+和O2,pH减小,阴极发生还原反应,生成H2和OH-,pH值增大;
③B口生成氧气,C生成氢气。
(1)开关与a点相连接时形成的是原电池,铁为原电池的负极,失去电子,电极反应为:Fe-2e-=Fe2+;
(2)当开关与b点连接时,形成的装置是电解池,石墨与电源的正极相连为阳极,铁与电源的负极相连,为阴极;①阳离子向阴极移动,即Na+向B极移动;②A端为阳极,电解质溶液中的Cl-失去电子变成Cl2,Cl2能使淀粉KI试纸变成蓝色;③阴极上H+得到电子变成氢气,因此反应一段时间后向电解液中通入HCl可使其恢复到电解前的浓度;
(3)①电解硫酸钾溶液,阳极发生氧化反应,OH-被氧化生成O2,电极反应为:4OH--4e-=2H2O+O2↑;SO42-通过阴离子交换膜向阳极移动,钾离子通过阳离子交换膜向阴极移动,据电荷守恒,则通过阳离子交换膜的K+数大于通过阴离子交换膜的SO42-数;
②电解后生成的硫酸和KOH溶液的浓度均比原来的大,则b<a,d>c,又因为碱溶液pH大于酸溶液pH,则:b<a<c<d;
③B口生成氧气,C生成氢气,物质的量之比为1:2,则质量之比为32:4=8:1。


科目:高中化学 来源: 题型:
【题目】实验室用苯和浓硝酸、浓硫酸发生反应制取硝基苯的装置如下图所示。请回答下列问题:
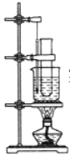
(1)反应需在55~60 ℃的温度下进行,图中给反应物加热的方法是________,
(2)在配制混合酸时先加_____________后加_____________;
(3)该反应的化学方程式是_____________________; 反应类型为:_______;
(4)反应完毕后,除去混合酸,所得粗产品用如下操作精制:①蒸馏 ②水洗 ③用干燥剂干燥 ④用10% NaOH溶液洗 ⑤水洗 正确的操作顺序是________。
A.①②③④⑤ B.②④⑤③①
C.④②③①⑤ D.②④①⑤③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值( )
为阿伏加德罗常数的值( )
A.标准状况下,将![]() 通入水中发生反应,转移的电子数为
通入水中发生反应,转移的电子数为![]()
B.常温常压下, 7g乙烯和丁烯的混合物含有的极性键数目为![]()
C.将![]() 与过量
与过量![]() 反应转移的电子数为
反应转移的电子数为![]()
D.标准状况下,![]() 中所含电子数为
中所含电子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属氟化物一般都具有高容量、高质量密度的特点。氟离子热电池是新型电池中的一匹黑马,其结构如图所示。下列说法正确的是

A. 图示中与电子流向对应的氟离子移动方向是(B)
B. 电池放电过程中,若转移1mol电子,则M电极质量减小12g
C. 电池充电过程中阳极的电极反应式为:B+3F--3e-=BiF3
D. 该电池需要在高温条件下工作,目的是将热能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
①在稀碱溶液中,溴苯难发生水解
②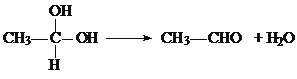
现有分子式为C10H10O2Br2的芳香族化合物X,其苯环上的一溴代物只有一种,其核磁共振氢谱图中有四个吸收峰,吸收峰的面积比为1:2:6:1,在一定条件下可发生下述一系列反应,其中C能发生银镜反应,E遇FeCl3溶液显色且能与浓溴水反应。
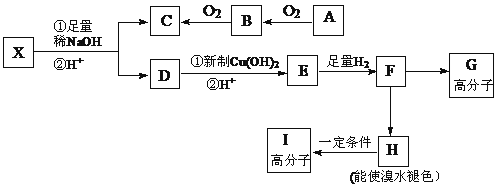
请回答下列问题:
(1)X中官能的名称是______________。
(2)F→H的反应类型是_________________。
(3)I的结构简式为___________________;
(4)E不具有的化学性质________(选填序号)
a.取代反应 b.消去反应
c.氧化反应 d.1molE最多能与2molNaHCO3反应
(5)写出下列反应的化学方程式:
①X与足量稀NaOH溶液共热的化学方程式:________________ ;
②F→G的化学方程式:____________________;
(6)同时符合下列条件的E的同分异构体共有_____ 种,其中一种的结构简式为________。
a.苯环上核磁共振氢谱有两种
b.不能发生水解反应
c.遇FeCl3溶液不显色
d.1molE最多能分别与1molNaOH和2molNa反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1 g物质完全燃烧时的反应热叫做该物质的热值。有以下能量转化图,下列说法不正确的是( )

A.转化Ⅰ的热化学方程式为:C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
B.转化Ⅱ的热化学方程式为:2CO(g)+O2(g)=2CO2(g) ΔH=-565.8 kJ·mol-1
C.由C→CO的热化学方程式为:2C(s)+O2(g)=2CO(g) ΔH=-110.6 kJ·mol-1
D.CO的热值:ΔH=-10.1 kJ·g-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向某浓度的H2A(二元弱酸)溶液中逐滴加入某浓度的KOH溶液,所得溶液中H2A、HA-、A2-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中正确的是( )
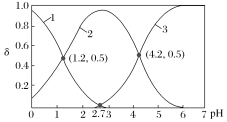
A.曲线1表示溶液中HA-的物质的量分数与pH的关系
B.pH=1.2时,溶液中c(K+)+c(H+)=c(OH-)+c(H2A)
C.pH=2.7至pH=4.2的过程中c(H2A)、c(A2-)、c(HA-)之和不变
D.pH=4时,溶液中存在下列关系:c(K+)>c(A2-)>c(HA-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学常见的短周期主族元素R、X、Y、Z、M的原子序数依次增大,它们占据三个周期。Y和M位于同主族,Y原子最外层电子数是电子层数的3倍。这五种元素组成一种离子化合物Q。取一定量Q溶于蒸馏水得到溶液,向溶液中滴加稀氢氧化钠溶液,产生沉淀与氢氧化钠溶液体积如图所示。下列说法不正确的是
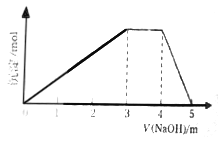
A. 简单的离子半径:M>Y>Z
B. 气态氢化物的热稳定性:Y>X
C. 由R、X、Y、M四种元素只组成一种盐
D. 最高价氧化物对应水化物的酸性:M>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素的一种同位素X的原子质量数为A,含N个中子,它与![]() 原子组成HmX分子.在a克HmX中所含质子的物质的量是( )
原子组成HmX分子.在a克HmX中所含质子的物质的量是( )
A. ![]() (A-N+m)molB.
(A-N+m)molB. ![]() (A-N)molC.
(A-N)molC. ![]() (A-N)molD.
(A-N)molD. ![]() (A-N+m)mol
(A-N+m)mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com