
【题目】在下列变化:①大气固氮,②硝酸银分解,③实验室制取氨气。按氮元素被氧化、被还原、既不被氧化又不被还原的顺序排列正确的是
A.①②③ B.②①③ C.③②① D.③①②
科目:高中化学 来源: 题型:
【题目】光电池是发展性能源。一种光化学电池的结构如图,当光照在表面涂有氯化银的银片上时,AgCl (s) ![]() Ag (s)+Cl(AgCl),[Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着Cl(AgCl)+e-=Cl- (aq),若将光源移除,电池会立即恢复至初始状态。下列说法不正确的是( )
Ag (s)+Cl(AgCl),[Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着Cl(AgCl)+e-=Cl- (aq),若将光源移除,电池会立即恢复至初始状态。下列说法不正确的是( )
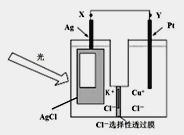
A. 光照时,电流由X流向Y
B. 光照时,Pt电极发生的反应为:2Cl-+2e-=Cl2↑
C. 光照时,Cl-向Pt电极移动
D. 光照时,电池总反应为:AgCl(s)+Cu+(aq)![]() Ag(s)+Cu2+(aq)+Cl-(aq)
Ag(s)+Cu2+(aq)+Cl-(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上有一种方法有效地开发利用CO2,是用CO2来生产燃料甲醇。为探究反应原理,进行如下实验,在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g);△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g);△H=-49.0kJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示。
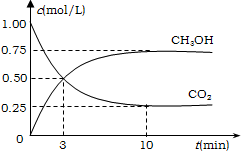
(1)从反应开始到平衡,氢气的平均反应速率v(CO2)= ________mol/(Lmin);
(2)氢气的转化率= ________;
(3)求此温度下该反应的平衡常数K=________;
(4)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是________
A.将H2O(g)从体系中分离出去
B.充入He(g),使体系压强增大
C.升高温度
D.再充入1mol CO2和3mol H2
(5)当反应达到平衡时,CO2的物质的量浓度为c1,然后向容器中再加入一定量CO2,待反应再一次达到平衡后,CO2的物质的量浓度为c2,则c1________ c2(填>、<、=)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用MnO2、KOH及KClO3为原料制取高锰酸钾的实验流程如下:
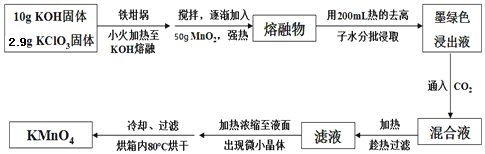
回答下列问题:
(1)实验中采用 (填“铁坩埚”或“瓷坩埚”)加热KOH和KClO3固体混合物。
(2)熔融时,MnO2转化为K2MnO4,KClO3转化为KCl,其反应的化学方程式为 。
(3)几种物质的溶解度曲线如图所示。
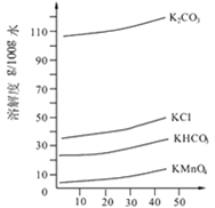
①通入CO2至pH为10~11,K2MnO4转化为KMnO4和MnO2。其反应的离子方程式为 。
②不能通入过量CO2的原因是 。
(4)趁热过滤的目的是 ;用冷水洗涤KMnO4晶体较好的原因是 。
(5)计算经过上述转化,最多可制得KMnO4的质量为 (结果保留2为小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容容器中,当下列物理量不变时,不能表明反应:A(s)+2B(g)C(g)+D(g)已达到平衡的是( )
A.混合气体压强
B.混合气体的密度
C.混合气体的平均相对分子质量
D.B的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 向50mL 18mol/L的H2SO4溶液中加入足量的铜片并加热,充分反应后,
转移电子的物质的量为( )
A.大于1.80 mol
B.等于0.90 mol
C.在0.90 mol和1.80 mol之间
D.小于0.90 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com