
【题目】 向50mL 18mol/L的H2SO4溶液中加入足量的铜片并加热,充分反应后,
转移电子的物质的量为( )
A.大于1.80 mol
B.等于0.90 mol
C.在0.90 mol和1.80 mol之间
D.小于0.90 mol
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】在下列变化:①大气固氮,②硝酸银分解,③实验室制取氨气。按氮元素被氧化、被还原、既不被氧化又不被还原的顺序排列正确的是
A.①②③ B.②①③ C.③②① D.③①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铝土矿主要含Al2O3和SiO2。某课题组以此为原料回收氧化铝,设计实验流程如下:
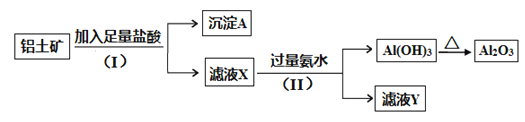
(1)步骤(I)中分离溶液和沉淀的操作名称是 。
(2)沉淀A中一定含有 (用化学式表示),该物质属于 (填“酸性”或“碱性”)氧化物。
(3)写出步骤(Ⅱ)中生成Al(OH)3的离子方程式 。
(4)实验室里用Na[Al(OH)4]溶液制取Al(OH)3最好选用 (填序号)。
A.NaOH溶液 B.稀硫酸 C.二氧化碳
(5)取5.4g铝土矿进行实验,最后得到氧化铝5.1g,则该铝土矿中铝的含量为__________(假设实验过程没有损失)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】难溶于水而且比水轻的含氧有机物是
①硝基苯 ②苯 ③溴苯 ④植物油 ⑤乙醇 ⑥乙酸乙酯 ⑦乙酸
A. ②④⑥⑦ B. ①②③④⑤ C. ④⑥ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A.2,2-二甲基丙烷也称异戊烷
B.乙苯的一溴代物共有四种
C.以淀粉为原料可制取乙酸乙酯
D.聚氯乙烯分子中含碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于氧化还原反应同时又是吸热反应的是
A.Ba(OH)2·8H2O与NH4Cl反应
B.铝与盐酸反应
C.灼热的炭与CO2反应
D.甲烷与O2的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除去杂质(括号内的物质为少量杂质)的方法中正确的是( )
A.乙烷(乙烯):光照条件下通入Cl2,气液分离
B.乙酸乙酯(乙酸):用饱和碳酸钠溶液洗涤、分液、干燥、蒸馏
C.CO2(HCl):气体通过盛有饱和Na2CO3溶液的洗气瓶
D.H2(O2):通过盛有灼热铜粉的玻璃管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能在水溶液中大量共存的是
A.Ca2+、SO42-、H+、HCO3- B.H+、NO3-、Cl-、SiO32-
C.K+、Fe2+、H+、NO3- D.K+、Na+、CO32-、SiO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铈、铬、钛、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。
(1)二氧化铈 (CeO2)在平板电视显示屏中有着重要应用。CeO2在稀硫酸和H2O2的作用下可生成Ce3+,写出该反应的化学方程式 ,CeO2在该反应中作__________剂。
(2)自然界中Cr主要以+3价和+6价存在,+6价的Cr能引起细胞的突变。现用亚硫酸钠溶液与0.1mol K2Cr2O7反应,将其+6价的Cr完全还原为+3价的铬,则消耗1mol/L亚硫酸钠溶液的体积为 L。
(3)钛(Ti)被誉为“二十一世纪的金属”,工业上在550℃时用钠与四氯化钛反应可制得钛,该反应的化学方程式是 。
(4)NiSO4·xH2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、锌、铁等元素)为原料获得.操作步骤如下:
①向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质(已知溶解度FeS>CuS)。请写出除去Cu2+的离子方程式 。
②对滤液Ⅱ先加H2O2再调pH。加H2O2的目的是 ,调pH的目的是 。
③滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com