
| A. | ①② | B. | ①③ | C. | ①④ | D. | ③④ |
分析 石墨为阴极,以Cu为阳极电解KI溶液,通电后,溶液中的H+、K+移向阴极,而H+的氧化性强于K+,所以H+得电子被还原,电极反应式为2H2O+2e-=H2↑+2OH-,破坏了水的电离平衡,使c(OH-)>c(H+),酚酞试液变红;I-和OH-移向阳极,而失电子能力Cu>I->OH-,故Cu失电子产生Cu2+,阳极发生反应:Cu-2e-=Cu2+,又由信息可知,同时又发生反应2Cu2++4I-=2CuI↓+I2,生成I2,I2遇淀粉变蓝,有白色CuI沉淀生成.
解答 解:石墨为阴极,以Cu为阳极电解KI溶液,通电后,溶液中的H+、K+移向阴极,而H+的氧化性强于K+,所以H+得电子被还原,电极反应式为2H2O+2e-=H2↑+2OH-,破坏了水的电离平衡,使c(OH-)>c(H+),酚酞试液变红;I-和OH-移向阳极,而失电子能力Cu>I->OH-,故Cu失电子产生Cu2+,阳极发生反应:Cu-2e-=Cu2+,又由信息可知,同时又发生反应2Cu2++4I-=2CuI↓+I2,生成I2,I2遇淀粉变蓝,有白色CuI沉淀生成,
①通电后,溶液中的H+、K+移向阴极,而H+的氧化性强于K+,所以H+得电子被还原,电极反应式为2H2O+2e-=H2↑+2OH-,破坏了水的电离平衡,使c(OH-)>c(H+),酚酞试液变红,故①正确;
②阳极Cu失电子产生Cu2+,生成Cu2+与I-能反应产生I2、CuI,I2遇淀粉变蓝,故②正确;
③阳极发生反应:Cu-2e-=Cu2+,生成Cu2+与I-能反应产生I2、CuI,I2遇淀粉变蓝,故③错误;
④阳极发生反应:Cu-2e-=Cu2+,又由信息可知,同时又发生反应2Cu2++4I-=2CuI↓+I2,故阳极反应为2Cu+4I--4e-=2CuI↓+I2,I2遇淀粉变蓝,故④错误;
故选A.
点评 本题考查电解原理,注意掌握离子放电顺序,明确电极反应式是关键,难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
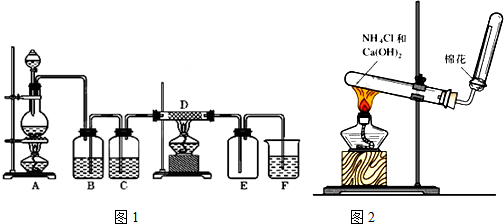
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
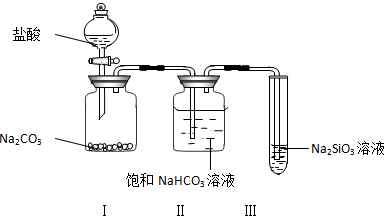
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 常温下0.1 mol•L-1的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,c(NH4+) 由大到小的顺序为②>①>③ | |
| B. | 常温下0.4 mol•L-1CH3COOH溶液和0.2 mol•L-1 NaOH溶液等体积混合后溶液显酸性,则溶液中粒子浓度由大到小的顺序为c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) | |
| C. | 0.1 mol•L-1 Na2CO3溶液与0.2 mol•L-1 NaHCO3溶液等体积混合所得溶液中:c(CO32-)+2c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) | |
| D. | 0.1 mol•L-1的氨水与0.05 mol•L-1 H2C2O4溶液等体积混合所得溶液中:c(NH4+)+c(NH3•H2O)=2c(C2O42-)+2c(HC2O4-)+2c(H2C2O4) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ②⑤ | D. | ⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | bd | B. | bc | C. | ad | D. | 只有d |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水中通入一定量的SO2气体可增强氯水的漂白性 | |
| B. | 因为SO2具有漂白性,所以它能使品红溶液、酸性高锰酸钾溶液褪色 | |
| C. | 已知酸性:H2SO4>HClO,则SO2通入漂白粉溶液中可生成次氯酸 | |
| D. | 紫色石蕊试液中通入SO2,溶液变红后不褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com