
| V |
| Vm |
| m |
| M |
| 1 |
| 2 |
| N |
| NA |
| 9.03×1023 |
| 6.02×1023mol-1 |
| 3g |
| 12g/mol |
| 0.25mol |
| 2 |
| 3.01×1023 |
| 6.02×1023mol-1 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
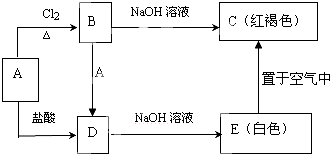 某金属A及其化合物之间有如下转化关系.
某金属A及其化合物之间有如下转化关系.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子序数:Z>W>X>Y |
| B、X、Y、Z、W形成的单质最多有6种 |
| C、X元素最高价氧化物对应水化物的化学式为:HXO3 |
| D、四种元素的气态氢化物中,W的气态氢化物最稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(NH4)2SO4的大量使用可能造成土壤的碱化 |
| B、磷肥的大量使用可能造成水体富营养化 |
| C、农药的使用可能影响害虫与其天敌之间的生态平衡 |
| D、家蚕吞食喷洒过农药的桑叶,可能引起中毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若把H2S分子写成H3S分子,违背了共价键的饱和性 |
| B、s轨道和p轨道重叠可以形成π键 |
| C、所有共价键都有方向性 |
| D、两个原子之间形成共价键时,可形成多个σ键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验组 | 温度℃ | 起始量/molm] | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.
某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.| 实验操作 | 实验现象 | 实验结论 | |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水 | 猜想a、c不成立,猜想b成立. | |
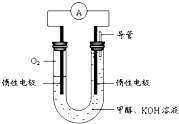
| 探究 | ①用带火星的木条伸入过氧化钠与水反应的试管中 | 木条复燃 | 生成物有 |
| ②往①试管内的溶液中滴加 | 生成物有氢氧化钠 |
| 实验操作 | 实验现象 | 实验结论 |
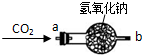
| ①将CO2从a口处通入装置内,再把带火星的木条放在装置b口处 | 木条复燃 | CO2在常温下能与过氧化钠反应,该反应的化学方程式为: |
| ②取出充分反应后的固体生成物于试管中,往试管内滴加稀盐酸,将生成的氢气通入澄清石灰水中 | 有气泡产生 石灰水变浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com