
����Ŀ���ϳɰ���ҵ���ִ�ũҵ��������ҵ�У�������Ҫ�ĵ�λ����֪��N2��g��+3H2��g��![]() 2NH3��g����H=��92kJ��mol��1��
2NH3��g����H=��92kJ��mol��1��
��1�������йظ÷�Ӧ���ʵ���������ȷ���� ��
a�������¶ȿ����������Ӱٷ������ӿ췴Ӧ����
b������ѹǿ�����������Ӱٷ����������Լӿ췴Ӧ����
c��ʹ�ô�������ʹ��Ӧ�����ƽ���������ߣ��ӿ췴Ӧ����
d��������һ��������£����������ı������С���Է�Ӧ����������Ӱ��
��2���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=_________________��
��3��ij�¶��£�����10 mol N2��30 mol H2 �������Ϊ10 L���ܱ������ڣ���Ӧ�ﵽƽ��״̬ʱ����û�������а����������Ϊ20%������¶��·�Ӧ��K= ���÷�����ʾ����
��4�����ںϳɰ���Ӧ���ԣ������й�ͼ��һ����ȷ����_____________��
a. b��
b�� c.
c.
���𰸡���1��abd
��2��![]() ��
��![]()
��3��![]() Lmol-1 ��4��ab
Lmol-1 ��4��ab
��������
�����������1��a�������¶ȣ�����ʹ��ͨ���ӻ��������Ϊ����ӣ�a��ȷ��b������ѹǿ������ʹ��ͨ���ӻ����������˻���Ӱٷ������䣬����������λ����ڻ��������b��ȷ��c������ֻ�ܽ��ͷ�Ӧ�Ļ�ܣ����ܸı䷴Ӧ������������������c����d��������һ��������£����������ı����ԽС����Ӧ����Խ�죬d��ȷ����ѡabd����2��N2��g�� + 3 H2��g�� ![]() 2 NH3��g����ƽ�ⳣ��K =
2 NH3��g����ƽ�ⳣ��K = ![]() ��
��![]() ����3���赪���ı仯Ũ��Ϊxmol/L���������֪��N2��g����H2��g����NH3��g����ƽ��Ũ�ȷֱ���1��x��mol/L����3��3x��mol/L��2xmol/L����ƽ���ǰ������������ =
����3���赪���ı仯Ũ��Ϊxmol/L���������֪��N2��g����H2��g����NH3��g����ƽ��Ũ�ȷֱ���1��x��mol/L����3��3x��mol/L��2xmol/L����ƽ���ǰ������������ = ![]() = 20%����ã�x=1/3����N2��g����H2��g����NH3��g����ƽ��Ũ�ȷֱ�2/3mol/L��2mol/L��2/3mol/L��ƽ�ⳣ��K =
= 20%����ã�x=1/3����N2��g����H2��g����NH3��g����ƽ��Ũ�ȷֱ�2/3mol/L��2mol/L��2/3mol/L��ƽ�ⳣ��K = ![]() =
=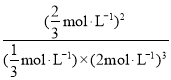 =
= ![]() Lmol-1����4��a��ʹ�ô������ܼӿ췴Ӧ���ʣ�������ʹƽ���ƶ���������ȹ���ƽ����������ƽ��ת���ʱ��ֲ��䣬a��ȷ��b�����ȹ���ƽ�����֪��ͼ��T2 > T1�������ܼӿ췴Ӧ���ʣ���ƽ�������ȷ�����淴Ӧ�����ƶ������������������С����ͼ��һ�£�b��ȷ��c���ӷ�Ӧ��ʼ���ﵽƽ�⣬��ӦN2��g�� + 3 H2��g��
Lmol-1����4��a��ʹ�ô������ܼӿ췴Ӧ���ʣ�������ʹƽ���ƶ���������ȹ���ƽ����������ƽ��ת���ʱ��ֲ��䣬a��ȷ��b�����ȹ���ƽ�����֪��ͼ��T2 > T1�������ܼӿ췴Ӧ���ʣ���ƽ�������ȷ�����淴Ӧ�����ƶ������������������С����ͼ��һ�£�b��ȷ��c���ӷ�Ӧ��ʼ���ﵽƽ�⣬��ӦN2��g�� + 3 H2��g�� ![]() 2 NH3��g�����������ʵı仯Ũ��֮�ȵ���ϵ��֮�Ȼ�1��3��2����ͼ��H2��NH3�ı仯Ũ�ȼ�����ȣ�c����ѡab��
2 NH3��g�����������ʵı仯Ũ��֮�ȵ���ϵ��֮�Ȼ�1��3��2����ͼ��H2��NH3�ı仯Ũ�ȼ�����ȣ�c����ѡab��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������£���ӦN2��g����3 H2��g�� ![]() 2 NH3��g�����ܱ������дﵽƽ��״̬����������ƽ��Ħ������Ϊ
2 NH3��g�����ܱ������дﵽƽ��״̬����������ƽ��Ħ������Ϊ![]() ��N2��NH3��Ũ�Ⱦ�Ϊc mol/L�������������ݻ�ѹ��Ϊԭ����
��N2��NH3��Ũ�Ⱦ�Ϊc mol/L�������������ݻ�ѹ��Ϊԭ����![]() �����ﵽ��ƽ��ʱ������˵������ȷ������ ��
�����ﵽ��ƽ��ʱ������˵������ȷ������ ��
A���µ�ƽ����ϵ�У�N2��Ũ��С��2 c mol/L����c mol/L
B���µ�ƽ����ϵ�У�NH3��Ũ��С��2 c mol/L����c mol/L
C���µ�ƽ����ϵ�У���������ƽ��Ħ������С��![]()
D���µ�ƽ����ϵ�У�������ܶ���ԭƽ����ϵ��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ƽ����ϵmA (g) +nB (g) ==C (g) +gD (g)����H <0�����н����д������
A. ���¶Ȳ��䣬�������������С��ԭ����һ�룬��ʱA��Ũ��Ϊԭ����2.1������m+n<p+q
B. ���¶Ȳ��䣬ѹǿ����ԭ����2�����ﵽ��ƽ��ʱ�������һ����ԭ����1/2ҪС
C. ��m+n=p+q����������a mol�����ƽ����ϵ���ټ���a mol��B���ﵽ��ƽ��ʱ������������ʵ�������2a
D. ��ƽ��ʱ��A��B��ת������ȣ�˵����Ӧ��ʼʱ��A��B�����ʵ���֮��Ϊm: n
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˳�ȥ������Ca2+��Mg2+��SO42-����ɳ���ɽ���������ˮ��Ȼ������������������
������ ���ӹ�����NaOH ������������ ���ӹ���Na2CO3��Һ ���ӹ���BaCl2��Һ
������ȷ�IJ���˳����
A���٢ܢڢݢ� B���ܢ٢ڢݢ�
C���ڢݢܢ٢� D���ݢ٢ܢڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˷�ֹǹ֧���⣬����ǹ֧�ĸ����������NaNO2��NaOH�Ļ����Һ�н��л�ѧ����ʹ���������������Fe3O4�����ܵı����㡪����������������̿������л�ѧ����ʽ��ʾ��
��3Fe��NaNO2��5NaOH===3Na2FeO2��H2O��NH3��
��![]() Na2FeO2��
Na2FeO2��![]() NaNO2��
NaNO2��![]() H2O��
H2O��![]() Na2Fe2O4��
Na2Fe2O4��![]() NH3����
NH3����![]() NaOH
NaOH
��Na2FeO2��Na2Fe2O4��2H2=Fe3O4��4NaOH
��ش��������⣺
(1)��ƽ��ѧ����ʽ�ڣ�������ǰ�Ļ�ѧ����������Ϊ______��
(2)������Ӧ���л�ԭ��Ϊ______������ԭ����______������1 mol Na2FeO2���ɣ���Ӧ������________mol���ӷ���ת�ơ�
(3)���ڡ��������Ĺ��̣�����˵����ȷ����________(����ĸ)��
A���ù��̲��������Ⱦ
B����Ӧ�����ɵ��������������п���ʴ����
C����Ӧ�٢ڢ۾���������ԭ��Ӧ
D����Ӧ�٢��е���������ΪNaNO2
(4)�������Һ��NaOHŨ�ȹ����������ĺ�Ȼ��С����ԭ����_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ʒ�������ǵĹ��Һ����������������ѣ���ͳ���ҹ�Ŀǰ��������Ա��80�������������꣬�����Ǵ�����dz��ں����մȾ��Ʒ�ġ��������֪ʶ�ж�����������һ�������ڶ�Ʒ����
A. ���� B. ��� C. ���� D. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������FeCl3��Һ�ֱ��������Һ���У����γɽ�����ǣ� ��
A.��ˮ
B.��ˮ
C.NaOHŨ��Һ
D.NaClŨ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������һ���ܴ���������ǣ� ��
A.���д���Ba2+����Һ�У�Cl��K+��SO42����CO32��
B.���д���H+����Һ�У�Mg2+��Na+��HCO3����SO42��
C.���д���OH������Һ�У�NH4+��NO3��SO42����CO32��
D.���д���Na+����Һ�У�H+��K+��SO42����NO3��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com