
| A、铁粉投醋酸溶液中:Fe+2H+=Fe2++H2↑ |
| B、Cl2溶于水:Cl2+H2O=2H++Cl-+ClO- |
| C、氢氧化钡溶液中滴加硫酸氢钠溶液至恰好为中性:Ba2++SO42-+2OH-+2H+=BaSO4↓+2H2O |
| D、向饱和澄清石灰水中加入纯碱溶液:Ca(OH)2+CO32-=CaCO3↓+2OH- |


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
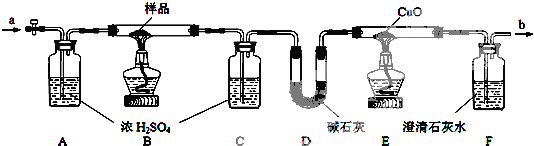
| 样品的质量 | C装置增重 | D装置增重 | E装置减轻 |
| 12.6g | 5.4g | 4.4g | 1.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解出的锂与水反应放出的H2 |
| B、在高温时阳极放出的Cl2与水作用放出的O2 |
| C、电解时产生的无色气体O2 |
| D、电解前LiCl加热时已发生水解,电解时产生的H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某课外活动小组利用如图所示的装置进行乙醇的催化氧化实验制取乙醛 (试管丙中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的铜丝,约lmin后鼓入空气.请填写下列空白:
某课外活动小组利用如图所示的装置进行乙醇的催化氧化实验制取乙醛 (试管丙中用水吸收产物),图中铁架台等装置已略去.实验时,先加热玻璃管中的铜丝,约lmin后鼓入空气.请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇中含有少量水可加入生石灰再蒸馏制得无水乙醇 |
| B、蔗糖水解用浓硫酸作催化剂 |
| C、在鸡蛋白溶液中加入浓HNO3,微热后会生成黄色物质 |
| D、油脂皂化反应后,反应混合物中加入食盐可将肥皂分离出来 |
| E、植物油和裂化汽油可用溴水鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com