
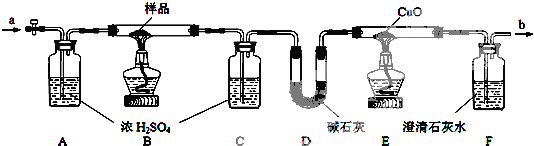
| 样品的质量 | C装置增重 | D装置增重 | E装置减轻 |
| 12.6g | 5.4g | 4.4g | 1.6g |
| 5.4g |
| 18g/mol |
| 4.4g |
| 44g/mol |
| 1.6g |
| 16g/mol |
| ||
| 9.6g |
| 16g/mol |


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案科目:高中化学 来源: 题型:
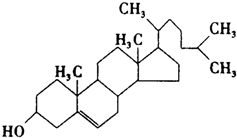
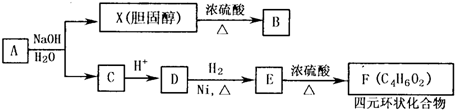
查看答案和解析>>
科目:高中化学 来源: 题型:
 Fenton法常用于处理含难降解有机物的工业废水,通常先调节好Fe2+等离子的浓度,再向废水中加入H2O2,所产生的羟基自由基(Fe2++H2O2→Fe3++OH-+HO?)能氧化降解污染物.如:降解废水中丙二醇(分子式C3H8O2)的反应为:C3H8O2+8H2O2
Fenton法常用于处理含难降解有机物的工业废水,通常先调节好Fe2+等离子的浓度,再向废水中加入H2O2,所产生的羟基自由基(Fe2++H2O2→Fe3++OH-+HO?)能氧化降解污染物.如:降解废水中丙二醇(分子式C3H8O2)的反应为:C3H8O2+8H2O2| FeSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某纯碱样品中含有少量氯化钠杂质,为了测定此样品纯度,甲同学设计了如图所示装置和实验方案.实验步骤如下:
某纯碱样品中含有少量氯化钠杂质,为了测定此样品纯度,甲同学设计了如图所示装置和实验方案.实验步骤如下:| 序号 | 改进意见 | 缺少时的影响 |
| ① | ||
| ② | ||
| ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁粉投醋酸溶液中:Fe+2H+=Fe2++H2↑ |
| B、Cl2溶于水:Cl2+H2O=2H++Cl-+ClO- |
| C、氢氧化钡溶液中滴加硫酸氢钠溶液至恰好为中性:Ba2++SO42-+2OH-+2H+=BaSO4↓+2H2O |
| D、向饱和澄清石灰水中加入纯碱溶液:Ca(OH)2+CO32-=CaCO3↓+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
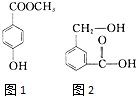 分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质有广泛用途.
分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质有广泛用途.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com