
����̫���ֽܷ�ˮ����H2���ڴ���������H2��CO2��Ӧ�ϳ�CH3OH����������ֱ���Լ״�Ϊȼ�ϵ�ȼ�ϵ�ء���֪��H2(g)+1/2O2(g)=H2O(l) ��H=��285.8 kJ��mol��1��CH3OH(l)+ 3/2O2(g)= CO2 (g)+ 2H2O(l) ��H=��726.5 kJ��mol��1��CO(g) +1/2O2(g)= CO2 (g) ��H=��283.0 kJ��mol��1��
��ش��������⣺
�� ��̫���ֽܷ�18gˮ����Ҫ���ĵ�����Ϊ kJ��
�� Һ̬CH3OH����ȫȼ������CO��Һ̬H2O���Ȼ�ѧ����ʽΪ ��
�� CO2�ϳ�ȼ��CH3OH��̼���ŵ��·������ݻ�Ϊ2 L���ܱ������У���2 mol CO2��6 mol H2����CO2��H2�ϳɼ״�����Ӧʽ��CO2(g)��3H2(g) CH3OH(g)��H2O(g)���������������������£������¶ȶԷ�Ӧ��Ӱ�죬ʵ��������ͼ��ʾ(ע��T1��T2������300 ��)��
CH3OH(g)��H2O(g)���������������������£������¶ȶԷ�Ӧ��Ӱ�죬ʵ��������ͼ��ʾ(ע��T1��T2������300 ��)��
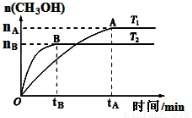
������˵����ȷ����
A���¶�ΪT2ʱ���ӷ�Ӧ��ʼ��ƽ�⣬���ɼ״���ƽ������Ϊ: v(CH3OH)��nB/tB mol��(L��min)��1
B��T2��T1��T2ƽ��ʱ���״��������٣����Ը÷�ӦΪ���ȷ�Ӧ
C���÷�Ӧ��T2ʱ��ƽ�ⳣ����T1ʱ��ƽ�ⳣ����
D������A��ķ�Ӧ��ϵ��T1�䵽T2��ƽ�������ƶ�
�����жϸ÷�Ӧ�Ѵﻯѧ��Ӧ�ȱ�־���� ������ĸ��
A��H2�İٷֺ������ֲ���
B��������CO2 Ũ����H2Ũ��֮��Ϊ1: 3
C�������л��������ܶȱ��ֲ���
D��CO2����������CH3OH�����������
�ȿ�ѧ��������CO2�ġ����ת���������о����罫CO2��H2�������1��4�������ͨ�뷴Ӧ�����ʵ������£���Ӧ�ɻ��һ����Դ��������»�ѧ����ʽ������֪��������Դ��
CO2��4H2  2H2O �� ��
2H2O �� ��
�� ��ֱ���Լ״�Ϊȼ�ϵ�ȼ�ϵ���У��������ҺΪ���ԣ��ܷ�ӦʽΪ��2CH3OH + 3O2��2CO2��4H2O���������ķ�ӦʽΪ �������ķ�ӦʽΪ ��
(1) 285.8 ��3�֣� �� CH3OH(l) + O2(g)��CO(g) + 2H2O(l) ��H=��443.5 kJ��mol��1��3�֣�
�� �� BD��2�֣� �� A ��2�֣� (4) CH4 ��2�֣�
�� 4H++O2+4e- = 2H2O��2�֣��� CH3OH+H2O-6e- = CO2+6H+��2�֣�
��������
�����������1����H2��g����ȼ���ȡ�HΪ-285.8kJ?mol-1֪��1molH2��g����ȫȼ������1molH2O��l���ų�����285.8kJ�����ֽ�1mol H2O��l��Ϊ1mol H2��g�����ĵ�����Ϊ285.8kJ����ֽ�18gˮ��1mol H2O��l�����ĵ�����Ϊ285.8kJ��
��2����CO��g����CH3OH��l����ȼ���ȡ�H�ֱ�Ϊ-283.0kJ?mol-1��-726.5kJ?mol-1����
��CO��g��+1/2O2��g��=CO2��g����H=-283.0kJ?mol-1����CH3OH��l��+3/2O2��g��=CO2��g��+2 H2O��l����H=-726.5kJ?mol-1���ɸ�˹���ɿ�֪�â�-�ٵ÷�ӦCH3OH��l��+O2��g��=CO��g��+2 H2O��l����
�÷�Ӧ�ķ�Ӧ�ȡ�H=-726.5kJ?mol-1-��-283.0kJ?mol-1������443.5kJ?mol-1��
��3����A���а�����������ʵķ�����֪��Ӧ����=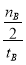 ��
�� mol/L?min����A����B������ӦΪ���ȷ�Ӧ���������ͼ�������֪��T2�ȴﵽƽ����T2��T1�����¶ȸ�ʱƽ��״̬CH3OH�����ʵ����٣���˵�����淴ӦCO2+3H2
mol/L?min����A����B������ӦΪ���ȷ�Ӧ���������ͼ�������֪��T2�ȴﵽƽ����T2��T1�����¶ȸ�ʱƽ��״̬CH3OH�����ʵ����٣���˵�����淴ӦCO2+3H2 CH3OH+H2O���淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ���÷�Ӧ�ġ�H��0����B��ȷ��C������ӦΪ���ȷ�Ӧ���������ͼ�������֪��T2�ȴﵽƽ�⣬��T2��T1���÷�Ӧ��T1ʱ��ƽ�ⳣ����T2ʱ�Ĵ�C����ȷ��D������A��ķ�Ӧ��ϵ��T1�䵽T2���¶����ߣ�����Ӧ���ȣ���ƽ�����淴Ӧ�����ƶ���D��ȷ����ѡBD��
CH3OH+H2O���淴Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ���÷�Ӧ�ġ�H��0����B��ȷ��C������ӦΪ���ȷ�Ӧ���������ͼ�������֪��T2�ȴﵽƽ�⣬��T2��T1���÷�Ӧ��T1ʱ��ƽ�ⳣ����T2ʱ�Ĵ�C����ȷ��D������A��ķ�Ӧ��ϵ��T1�䵽T2���¶����ߣ�����Ӧ���ȣ���ƽ�����淴Ӧ�����ƶ���D��ȷ����ѡBD��
����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬����A��H2�İٷֺ������ֲ������˵����Ӧ�ﵽƽ��״̬��A��ȷ��B��ƽ��ʱŨ�Ȳ��ٷ����仯���������ʵ�Ũ��֮�䲻һ����Ȼ�����ij�ֹ�ϵ�����������CO2 Ũ����H2Ũ��֮��Ϊ1: 3����˵����Ӧ�ﵽƽ��״̬��B����ȷ��C���ܶ��ǻ�����������������ݻ��ı�ֵ���ڷ�Ӧ�������������ݻ�ʼ���Dz���ģ���������л��������ܶȱ��ֲ��䲻��˵����Ӧ�ﵽƽ��״̬��C����ȷ��D��CO2����������CH3OH�������ʷ���һ�£���������֮�ȵ�����Ӧ�Ļ�ѧ������֮�ȿ�֪�����ߵ�����ʼ������ȵģ�����˵���ﵽƽ����̬��D����ȷ����ѡA��
��4������ԭ���غ��֪����Ӧ������һ���������Ǽ��飬��CO2��4H2  CH4��2H2O��
CH4��2H2O��
��5��ֱ���Լ״�Ϊȼ�ϵĵ���У��������ҺΪ���ԣ����������õ����ӣ��������缫��ӦʽΪ4H++O2+4e- = 2H2O���״�ȼ�ϵ�أ�ȼ���ڸ���ʧ���ӷ���������Ӧ�������ķ�ӦʽΪCH3OH+H2O-6e- = CO2+6H+��
���㣺�������������ƽ��״̬��Ӱ�졢ƽ��״̬�ж��Լ����淴Ӧ���йؼ��㡢�缫��Ӧʽ����д��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�콭����У������һ��������ѧ�Ծ��������棩 ���ͣ������
��8�֣��Կ��淴ӦaA(g)��bB(g)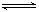 cC(g)��d��(g)�ﵽƽ��ʱ�������ʵ����ʵ���Ũ���������¹�ϵ��
cC(g)��d��(g)�ﵽƽ��ʱ�������ʵ����ʵ���Ũ���������¹�ϵ��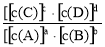 =K(Ϊһ����)��K��Ϊ��ѧƽ�ⳣ�����䷴Ӧ��Kֵֻ���¶��йء����з�Ӧ��CO(g)��H2O(g)
=K(Ϊһ����)��K��Ϊ��ѧƽ�ⳣ�����䷴Ӧ��Kֵֻ���¶��йء����з�Ӧ��CO(g)��H2O(g)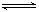 CO2(g)��H2(g) ��H����Q kJ��mol��1����850��ʱ��K��1��
CO2(g)��H2(g) ��H����Q kJ��mol��1����850��ʱ��K��1��
��1���������¶ȵ�950��ʱ���ﵽƽ��ʱK 1(����ڡ���С�ڡ����ڡ�)��
��2��850��ʱ������һ�ݻ��ɱ���ܱ�������ͬʱ����1.0 mol CO��3.0 mol H2O��1.0 mol CO2��x mol H2���ٵ�x��5.0ʱ������ƽ���� (�����Ӧ�����淴Ӧ��)�����ƶ���
����Ҫʹ������Ӧ��ʼʱ������Ӧ������У���xӦ����������� ��
��3����850��ʱ������x��5.0��x��6��0���������ʵ�Ͷ�ϲ��䣬��������Ӧ�ﵽƽ����H2����������ֱ�Ϊa����b������a b(����ڡ���С�ڡ����ڡ�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������Э����߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��֪�� C(s)��O2(g)��CO2(g) ��H����393��5 kJ/mol
2CO(g)��O2(g)��2CO2(g) ��H����566 kJ/mol
TiO2(s)��2Cl2(g)��TiCl4(s)��O2(g) ��H��+141 kJ/mol
��TiO2(s)��2Cl2(g)��2C(s)��TiCl4(s)��2CO(g) ��H�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������Э����߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ʷ��������ȷ����
| A | B | C | D |
ǿ����� | HCl | FeCl3 | H3PO4 | HClO |
������� | HF | CH3COOH | BaSO4 | Ba(OH)2 |
�ǵ���� | NH3 | Cu | H2O | C2H5OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������Э����߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��Ӧ2CO��g��=2C��s��+O2��g���ġ�HΪ��ֵ����SΪ��ֵ�����H�͡�S�����¶ȶ��䣬����˵����ȷ����
A�����������Է�����
B�����������Է�����
C�������²����Է����У����������Է�����
D���κ��¶��¶������Է�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����ظ߶���ѧ�����е��в��Ի�ѧ�Ծ��������棩 ���ͣ������
��Ҫ������������⣺
��ij�л���ļ���ʽ�� ����д������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ ��
����д������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ ��
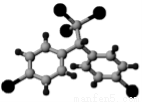
��DDT����ϳɵĵ�һ���л���ũҩ������ӽṹ���ģ����ͼ��ʾ������������ʵĺ˴Ź���1H��ͼ���� �����շ塣
��F��G��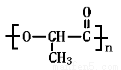 �� ���ճ������г��õ����ֺϳɸ߷��Ӳ��ϣ�����ij�������з�Ӧ�õ���
�� ���ճ������г��õ����ֺϳɸ߷��Ӳ��ϣ�����ij�������з�Ӧ�õ���
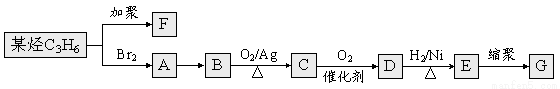
��ش��������⣺
��F�Ľṹ��ʽΪ ��
��C�����������ŵ�����Ϊ ���� �ǣ����ԲⶨD�����������š�
��A��B�Ļ�ѧ����ʽΪ ��
����֪ 2RCH(OH)COOH 2H2O +
2H2O + 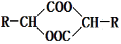
��ο���Ŀ�еĺϳ�;�������ϳ� ����ʼԭ�ϵ�ij���Ľṹ��ʽΪ �������� ����Ӧ�����Ժϳɲ��
����ʼԭ�ϵ�ij���Ľṹ��ʽΪ �������� ����Ӧ�����Ժϳɲ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����ظ߶���ѧ�����е��в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���ӡ�315�ر��ж����ع��˺���һЩ�ط������⾫���¼��������⾫�������彡�������Σ������֪ij�֡����⾫�����п�������(Clenbuterol)����ṹ����ͼ�������йؿ���������������ȷ����
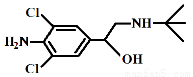
A�������ʵķ���ʽΪC12H17ON2Cl
B�������ʲ���������
C������������FeCl3��Һ������ɫ��Ӧ
D�������ʷ��Ӽ䶼�����γ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ���������и߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��������٤��������ֵ������ڷ�Ӧ��C2H2 (g) + 5/2O2(g)��2CO2(g) + H2O(l) ��H����1300 kJ?mol-1���Ȼ�ѧ����ʽ��˵������ȷ����
A����10NA������ת��ʱ���÷�Ӧ�ų�1300kJ������
B����NA��ˮ����������ΪҺ��ʱ������1300kJ������
C����2NA��̼�����õ��Ӷ�����ʱ���ų�1300kJ������
D����8NA��̼�����õ��Ӷ�����ʱ���ų�1300kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�������Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ijԪ�ص�ԭ��������Ӳ��Ų���6s26p4����Ԫ�ػ��仯���ﲻ���ܾ��е�������
A����Ԫ�ص��ʿ����ǵ���
B����Ԫ�ص�����ϼ۳ʣ�6��
C����Ԫ������������Ӧ������̬�⻯��
D����Ԫ�ؼ۵��ӹ������2��δ�ɶԵ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com