
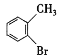
【题目】2020年2月,国家卫生健康委办公厅、国家中医药管理局办公室联合发出《关于印发新型冠状病毒肺炎诊疗方案(试行第六版)的通知》。此次诊疗方案抗病毒治疗中增加了有机物G,G是一种医药中间体,可通过如图所示路线合成。A是石油化工的重要产品且分子中所有原子在同一平面内,H的分子式是C7H8。
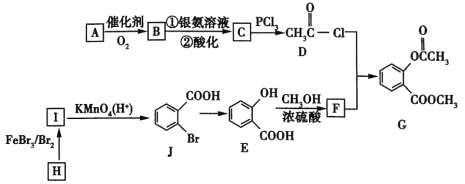
已知:![]() 。
。
回答下列问题。
(1)A的结构简式是___________。
(2)H→I的化学方程式为__________,B与银氨溶液反应的化学方程式是__________。
(3)C→D的反应类型是______,I→J的反应类型是______。
(4)两个E分子在一定条件下发生分子间脱水生成一种环状酯的结构简式是_______________。
(5)满足以下条件的F的同分异构体(不含F)共有_________种。
①能与氯化铁溶液发生显色反应 ②分子中有—COO—结构 ③苯环上有两个取代基
【答案】CH2=CH2 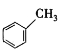 +Br2
+Br2![]()
 +HBr CH3CHO+2Ag(NH3)2OH
+HBr CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+3NH3+2Ag↓+H2O 取代反应 氧化反应
CH3COONH4+3NH3+2Ag↓+H2O 取代反应 氧化反应 ![]() 11
11
【解析】
A是石油化工的重要产品且分子中所有原子在同一平面内,则A是乙烯,结构简式是CH2=CH2,A催化氧化产生B能够发生银镜反应,则B是CH3CHO,B与银氨溶液水浴加热发生银镜反应,经酸化得到C是CH3COOH,C与PCl3发生取代反应产生D:![]() ,H的分子式是C7H8,由于在反应过程中物质结构不变,由J的结构逆推可知H是甲苯,结构简式是:
,H的分子式是C7H8,由于在反应过程中物质结构不变,由J的结构逆推可知H是甲苯,结构简式是:![]() ,甲苯与Br2在FeBr3催化下发生取代反应产生I为
,甲苯与Br2在FeBr3催化下发生取代反应产生I为 ,I被酸性KMnO4溶液氧化产生J:
,I被酸性KMnO4溶液氧化产生J: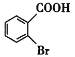 ,J发生取代反应产生E:
,J发生取代反应产生E: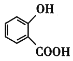 ,E与甲醇在浓硫酸催化下发生酯化反应产生F:
,E与甲醇在浓硫酸催化下发生酯化反应产生F: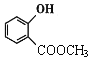 ,D、F发生取代反应产生G:
,D、F发生取代反应产生G: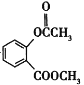 。
。
根据上述分析可知:A是CH2=CH2,B是CH3CHO,C是CH3COOH,D是![]() ,E是
,E是 ,F是
,F是 ,G是
,G是 ,H是
,H是![]() ,I是
,I是 ,J是
,J是 。
。
(1)A结构简式是CH2=CH2;
(2)H是![]() ,与Br2在FeBr3催化下发生取代反应产生
,与Br2在FeBr3催化下发生取代反应产生 和HBr,则H→I的化学方程式为:
和HBr,则H→I的化学方程式为: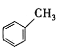 +Br2
+Br2![]()
 +HBr;
+HBr;
B是CH3CHO,含有醛基,与银氨溶液水浴加热发生氧化反应,醛基被氧化变为羧基,与溶液中的NH3反应产生CH3COONH4,则B与银氨溶液反应的化学方程式为:CH3CHO+2Ag(NH3)2OH![]() CH3COONH4+3NH3+2Ag↓+H2O;
CH3COONH4+3NH3+2Ag↓+H2O;
(3)C是乙酸,与PCl3发生取代反应产生D:![]() ;I是
;I是 与酸性高锰酸钾溶液发生氧化反应产生J:
与酸性高锰酸钾溶液发生氧化反应产生J:  ,因此I→J的反应类型是氧化反应;
,因此I→J的反应类型是氧化反应;
(4)E是 ,分子中含有-OH、-COOH,与浓硫酸混合加热,两个E分子发生分子间脱水生成一种环状酯和水,脱水时羧基脱去羟基,羟基脱去H原子,其余部分结合在一起,故该酯的结构简式是
,分子中含有-OH、-COOH,与浓硫酸混合加热,两个E分子发生分子间脱水生成一种环状酯和水,脱水时羧基脱去羟基,羟基脱去H原子,其余部分结合在一起,故该酯的结构简式是![]() ;
;
(5)F是 ,其同分异构体满足条件:①能与氯化铁溶液发生显色反应,说明含有酚羟基; ②分子中有—COO—结构;③苯环上有两个取代基,则可能的结构为:-OH、-COOCH3,或-OH、-OOCCH3,或-OH、-CH2COOH,或-OH、-CH2OOCH,每种情况在苯环上都存在邻、间、对三种不同位置,故符合条件的同分异构体(不包含F)有4×3-1=11种。
,其同分异构体满足条件:①能与氯化铁溶液发生显色反应,说明含有酚羟基; ②分子中有—COO—结构;③苯环上有两个取代基,则可能的结构为:-OH、-COOCH3,或-OH、-OOCCH3,或-OH、-CH2COOH,或-OH、-CH2OOCH,每种情况在苯环上都存在邻、间、对三种不同位置,故符合条件的同分异构体(不包含F)有4×3-1=11种。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】可逆反应2NO2![]() 2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成nmolO2的同时生成2nmolNO2
②单位时间内生成nmolO2的同时生成2nmolNO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
A.②③B.①④
C.①③④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.室温下,1 L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA
B.反应 5NH4NO3![]() 2HNO3+4N2↑ +9H2O 中,生成 28 g N2 时,转移的电子数目为3.75 NA
2HNO3+4N2↑ +9H2O 中,生成 28 g N2 时,转移的电子数目为3.75 NA
C.0.1 mo1·L-1 MgCl2溶液中含Cl-数为0.2NA
D.3.9 g Na2O2 晶体中含有的离子总数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( )

A. ①为简单立方堆积 ②为六方最密堆积 ③为体心立方堆积 ④为面心立方最密堆积
B. 每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个
C. 晶胞中原子的配位数分别为:①6,②8,③8,④12
D. 空间利用率的大小关系为:①<②<③<④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Ag++SCN-=AgSCN↓(白色)。实验室可通过如下过程测定所制硝酸银样品的纯度(杂质不参与反应)。
(1)称取2.000g制备的硝酸银样品,加水溶解,定容到100 mL。溶液配制过程中所用的玻璃仪器除烧杯、玻璃棒外还有_________。
(2)准确量取25.00 mL溶液,酸化后滴入几滴铁铵钒[NH4Fe(SO4)2]溶液作指示剂,再用0.100 mol·L-1 NH4SCN标准溶液滴定。滴定终点的实验现象为_________。终点时消耗标准溶液25mL,硝酸银样品纯度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁有δ、γ、α三种同素异形体,其晶胞结构如图所示,下列判断正确的是
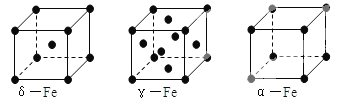
A. δ、γ、α铁晶体中存在金属阳离子和阴离子
B. γ—铁晶体晶胞中所含有的铁原子数为14
C. δ、α两种晶胞中铁原子的配位数之比为4∶3
D. 若α-Fe晶胞边长为a cm,γ-Fe晶胞边长为b cm,则两种晶体的密度比为b3∶a3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼氢化钠(NaBH4)具有优良的还原性,在有机化学和无机化学领域有着广泛的应用。利用硼精矿(主要成分为B2O3,含有少量Al2O3、SiO2、FeCl3等![]() 制取NaBH4的流程如图:
制取NaBH4的流程如图:

已知:偏硼酸钠(NaBO2)易溶于水,不溶于醇,在碱性条件下稳定存在,回答下列问题:
(1)写出加快硼精矿溶解速率的措施______![]() 写一种
写一种![]() 。
。
(2)操作1为______,滤渣主要成分为______。
(3)除硅铝步骤加入CaO而不加入CaCl2的原因有:①能将硅、铝以沉淀除去;②______.
(4)氢化镁(MgH2)中H元素的化合价为______;MgH2与NaBO2在一定条件下发生反应1,其化学方程式为:______。
(5)如图在碱性条件下,在阴极上电解NaBO2也可制得硼氢化钠,写出阴极室的电极反应式______。
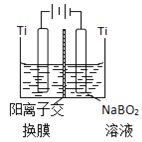
(6)硼氢化钠是一种强还原剂,碱性条件可处理电镀废液中的硫酸铜制得纳米铜,从而变废为宝,写出该反应的离子方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往2L密闭容器中充入NO2,在三种不同条件下发生反应:2NO2(g)2NO(g)+O2(g),实验测得NO2的浓度随时间的变化如下表![]() 不考虑生成N2O4)
不考虑生成N2O4)
0 | 10 | 20 | 30 | 40 | 50 | |
实验1/800 | 1.00 | 0.80 | 0.65 | 0.55 | 0.50 | 0.50 |
实验2/800 | 1.00 | 0.70 | 0.50 | 0.50 | 0.50 | 0.50 |
实验3/850 | 1.00 | 0.50 | 0.40 | 0.15 | 0.15 | 0.15 |
下列说法正确的是( )
A.实验2比实验1的反应容器内压强减小
B.实验2比实验l使用了效率更高的催化剂
C.实验1比实验3的平衡常数大
D.实验2和实验3可判断该反应是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了以Ni / Al2O3 为催化剂,由CO2和H2转化为产品CH4的反应历程,其示意图如下:

下列说法不正确的是
A. 总反应方程式为:CO2+4H2![]() CH4+2H2O
CH4+2H2O
B. 催化剂可有效提高反应物的平衡转化率
C. 在反应历程中,H―H键与C=O键断裂吸收能量
D. 反应过程中,催化剂参与反应,改变反应路径,降低反应的活化能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com