
| 反应 | 乙醇(mol) | 乙酸(mol) | 乙酯乙酯(mol) |
| 1 | 2 | 2 | 1.33 |
| 2 | 3 | 2 | 1.57 |
| 3 | 4 | 2 | x |
| 4 | 5 | 2 | 1.76 |
| c(H+) |
| c(CH3COOH) |
| C(H+) |
| C(CH3COOH) |


科目:高中化学 来源: 题型:
 (2010?长春一模)向一定量的K2CO3溶液中缓慢滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中各离子数目也相应地发生变化.溶液中各离子数目与图中四条曲线的对应关系完全正确的是( ) (2010?长春一模)向一定量的K2CO3溶液中缓慢滴加稀盐酸,并不断搅拌.随着盐酸的加入,溶液中各离子数目也相应地发生变化.溶液中各离子数目与图中四条曲线的对应关系完全正确的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
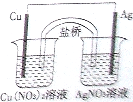 (2010?长春一模)用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U形管)构成一个原电池(如图).以下有关该原电池的叙述正确的是
(2010?长春一模)用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U形管)构成一个原电池(如图).以下有关该原电池的叙述正确的是查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com