
| A. | 直线形 | B. | 正四面体形 | C. | 锯齿形 | D. | 有支链的直线形 |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0~15 s 内用 I2 表示的平均反应速率为:v(I2)=0.001 mol•L-1•s-1 | |
| B. | c(HI)由 0.07 mol•L-1 降到 0.05 mol•L-1 所需的反应时间小于 10 s | |
| C. | 升高温度正反应速率加快,逆反应速率减慢 | |
| D. | 减小反应体系的体积,化学反应速率加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①<② | B. | ①>② | C. | ①=② | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
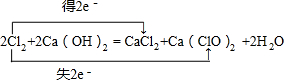 (并用双线桥标出电子转移的方向和数目),其中氧化产物为Ca(ClO)2(写化学式).
(并用双线桥标出电子转移的方向和数目),其中氧化产物为Ca(ClO)2(写化学式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 位于短周期的X元素的阳离子与Y元素的阴离子具有相同的电子层结构,则两元素的最高正化合价一定是X<Y | |
| B. | 对于某元素的单质,若它的氧化性弱,那么它的还原性一定强 | |
| C. | 热稳定性:AsH3<PH3<H2O<HF | |
| D. | 最外层电子数较少的金属元素,一定比最外层电子数较多的金属元素活泼性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
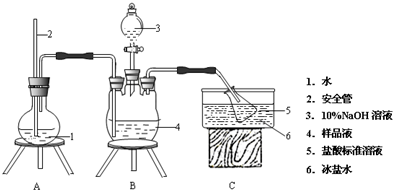
 已知:卤素的氢化物易溶于水.某同学采用如图所示装置研究氯气与甲烷反应.实验时,往U型管的左端装入甲烷和氯气(体积比为1:4)的混合气体,并将该装置放置在光亮处,让混合气体缓慢地反应一段时间.根据要求回答问题:
已知:卤素的氢化物易溶于水.某同学采用如图所示装置研究氯气与甲烷反应.实验时,往U型管的左端装入甲烷和氯气(体积比为1:4)的混合气体,并将该装置放置在光亮处,让混合气体缓慢地反应一段时间.根据要求回答问题: A.氢原子数为十二 B.一氯取代物只有一种结构.
A.氢原子数为十二 B.一氯取代物只有一种结构.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com