
下列说法正确的是
A、水晶是无色透明的晶体,可以制成硅太阳能电池
B、将FeCl3饱和溶液滴入沸水中,可以立即得到Fe(OH)3胶体
C、盛装NaOH溶液的试剂瓶用橡胶塞,不用玻璃塞
D、不能通过丁达尔效应来鉴别Fe(OH)3胶体和CuSO4溶液
科目:高中化学 来源:2014-2015学年河北省高三1月练习理综化学试卷(解析版) 题型:填空题
(16分)
Ⅰ、工业上用含有Cr2O72-和CrO42-的废水回收铬。其工艺流程如下:
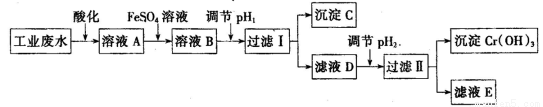
已知:①2 CrO42-(黄色)+2H+  Cr2O72-(橙色)+ H2O;
Cr2O72-(橙色)+ H2O;
②常温下,Ksp【Fe(OH)3】=1.0×10-38,Ksp【Cr(OH)3】=1.0×10-32;
③当离子浓度小于1.0×10-5 mol·L-1时,认为沉淀完全。
(1)下列选项中能说明反应2 CrO42-(黄色)+2H+  Cr2O72-(橙色)+ H2O达平衡状态的是_______(填选项字母)。
Cr2O72-(橙色)+ H2O达平衡状态的是_______(填选项字母)。
A.Cr2O72-和CrO42-的浓度相同
B.2v(Cr2O72-)= v(CrO42-)
C.溶液的颜色不变
D.溶液的PH不变
(2)为防止FeSO4溶液变质,在保存时需加入的试剂为 (填试剂名称)
(3)过滤操作中需要用到的玻璃仪器有
(4)FeSO4溶液与溶液A发生反应的离子方程式为
(5)沉淀C的化学式为 ,pH2的范围为
Ⅱ、铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。
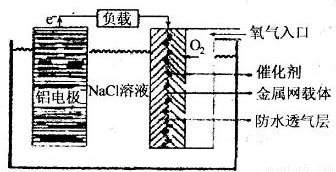
(6)该电池的总反应化学方程式为 ;
(7)某铝一空气电池的效率为50%,若用其作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液(假设溶液电解前后体积不变)中NaOH的浓度为0.3 mol·L-1,则该过程中消耗铝的质量为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省惠州市高三第三次调研考试化学试卷(解析版) 题型:选择题
下列实验操作和对应的现象、结论都正确的是
选项 | 操 作 | 现 象 | 结 论 |
A | 在滴有酚酞的Na2CO3溶液中加入BaC12溶液 | 红色褪去 | Na2CO3溶液中存在水解平衡 |
B | 将某气体通入品红溶液中 | 品红溶液褪色 | 该气体一定是SO2 |
C | 将铜板电路投入FeCl3溶液中 | 铜溶于FeCl3溶液 | 氧化性:Fe3+ > Cu2+ |
D | 向NaCl溶液滴少量AgNO3溶液,再滴加少量NaI溶液 | 先有白色沉淀,后变成黄色沉淀 | Ksp(AgI) >Ksp(AgCl) |
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:选择题
a、b、c、d是四种短周期的主族元素。a、b、d同周期,其中d的质子数最大;a、c同主族。a的原子结构示意图为: ;a与b形成化合物的电子式为:
;a与b形成化合物的电子式为: 。下列叙述正确的是
。下列叙述正确的是
A. 原子半径:a>c>d
B. 非金属性:c>a>d
C. 相应氢化物的沸点:d>c>a
D. c与a、c与b均能形成两种常见化合物
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列过程属于物理变化的是:
A.煤的气化 B.石油分馏 C.石油裂解 D.煤的直接液化
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省濉溪县高三第二次月考化学试卷(解析版) 题型:实验题
(8分)某化学兴趣小组设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数。

(1)m g铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是 、 。
(2)A中铁与浓硫酸在加热时反应的化学方程式为 。
(3)待A中不再逸出气体时,停止加热,拆下装置E并称重,装置E增重n g。则铁碳合金中铁的质量分数为 (用含m、n的表达式表示)。
(4)甲同学认为利用此装置测得铁的质量分数可能偏小,请写出其可能原因: 。乙同学认为利用此装置测得铁的质量分数可能偏大,请写出其可能原因: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省安庆五校联盟高三下学期3月联考理综化学试卷(解析版) 题型:选择题
在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应:X(g)+Y(g) 2Z(g) △H<0,一段时间后达到平衡。反应过程中测定的数据如下表:

下列说法不正确的是
A.该温度下此反应的平衡常数K=1.44
B.其他条件不变,升高温度,反应达到新平衡前V(逆)< V (正)
C.反应前2 min的平均速率v (Z)=4.0×10-3mol/(L·min)
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数不变
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南市高三上学期期末考试化学试卷(解析版) 题型:填空题
(8分)I.下列实验操作或对实验事实的描述中,正确的是________(填序号)。
①用量筒量取稀硫酸溶液8.0 mL;
②Fe(OH)3胶体与FeCl3溶液的混合物可用过滤的方法分离;
③用湿润的pH试纸测量某溶液pH时,测量值可能比真实值小;
④用碱式滴定管量取KMnO4溶液20.50 mL;
⑤在实验室中用锌和稀硫酸反应制氢气,为加快反应速率而不影响H2的品质,可向溶液中加适量Cu(NO3)2晶体。
Ⅱ.将某98%的浓硫酸样品敞口露置于空气中,放置24 h后,取出5 mL浓硫酸与18 mL 9 mol·L-1的NaOH溶液恰好完全中和。请回答下列问题:
(1)该硫酸样品露置24 h后,其物质的量浓度是___________mol·L-1。
(2)若分别用下列方法鉴别浓硫酸和稀硫酸,可以达到目的的是____________(填序号)。
a.常温下加入铜片
b.常温下加入铁片
c.常温下加入木炭
d.用玻璃棒各蘸取少许涂在滤纸上
(3)工业上利用过量氨水吸收硫酸工业尾气中的有害物质,请写出该过程中发生的一个反应的离子方程式_____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com