(2011?崇文区模拟)U、W、X、Y、Z都是短周期元素,且原子序数依次增大.其中U与W可形成三角锥形分子A,U与X可形成常温下呈液态的分子B,A、B均为10电子分子;Y元素原子的K层电子数与M层电子数相同;Z元素的单质、氧化物均为原子晶体.
请回答下列问题:
(1)Z元素在周期表中的位置
第三周期ⅣA族
第三周期ⅣA族
.W、X、Y、Z四种元素的原子半径由小到大的顺序是
O<N<Si<Mg
O<N<Si<Mg
(用元素符号表示).
(2)U与X形成的18电子化合物的电子式是
.
(3)ZX
2与NaOH溶液反应的化学方程式是
SiO2+2NaOH=Na2SiO3+H2O
SiO2+2NaOH=Na2SiO3+H2O
.
(4)你认为U、W、X元素形成的化合物之间
不能
不能
(填“能”或“不能”)发生如下反应:WX+WU
3→UWX
2+U
2X,得出此结论的理由是
在此反应关系中,只有失电子的物质,没有得电子的物质
在此反应关系中,只有失电子的物质,没有得电子的物质
.
(5)一定量的Y单质在足量二氧化碳中充分燃烧的化学方程式是
,将生成的全部固体与足量的热浓硝酸混合,充分反应后,产物中二氧化碳和二氧化氮共a L(标准状况),则Y单质的质量是
g(用含a的代数式表示).



 ,故答案为:
,故答案为: ;
;

 阅读快车系列答案
阅读快车系列答案 (2011?崇文区模拟)一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:
(2011?崇文区模拟)一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应: p C(g)+q D(g)达到平衡后,测得B的浓度为0.5
p C(g)+q D(g)达到平衡后,测得B的浓度为0.5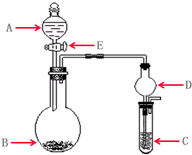 (2011?崇文区模拟)实验室需要少量某些气体时,通常使用快速的方法制备.下列几个实验可快速制取实验室所需的少量气体,并进行相关性质实验.(实验装置如图所示)
(2011?崇文区模拟)实验室需要少量某些气体时,通常使用快速的方法制备.下列几个实验可快速制取实验室所需的少量气体,并进行相关性质实验.(实验装置如图所示)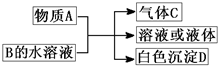 (2011?崇文区模拟)A、B、C、D均为中学化学常见物质,它们之间的反应关系如图所示.
(2011?崇文区模拟)A、B、C、D均为中学化学常见物质,它们之间的反应关系如图所示.